Lantus per il trattamento del diabete
Marchio: Lantus
Nome generico: insulina glargine
Forma di dosaggio: iniezione (Lantus NON deve essere diluito o miscelato con qualsiasi altra insulina o soluzione)
Contenuti:
Descrizione
Farmacologia clinica
Indicazioni e utilizzo
Controindicazioni
Avvertenze
Precauzioni
Reazioni avverse
Dosaggio e amministrazione
Come viene fornito
Lantus, insulina glargine (origine di rDNA), informazioni per il paziente (in inglese semplice)
Descrizione
Lantus® (iniezione di insulina glargine [origine rDNA]) è una soluzione sterile di insulina glargine da utilizzare come iniezione. L'insulina glargine è un analogo dell'insulina umana ricombinante che è un agente parenterale per abbassare la glicemia ad azione prolungata (fino a 24 ore di azione). (Vedere FARMACOLOGIA CLINICA). Il lantus è prodotto dalla tecnologia del DNA ricombinante utilizzando un ceppo di laboratorio non patogeno dell'Escherichia coli (K12) come organismo di produzione. L'insulina glargine differisce dall'insulina umana in quanto l'amminoacido asparagina in posizione A21 viene sostituito dalla glicina e due arginine vengono aggiunte al C-terminus della catena B. Chimicamente, è l'insulina 21A-Gly-30Ba-L-Arg-30Bb-L-Arg-umana e ha la formula empirica C267H404N72O78S6 e un peso molecolare di 6063. Ha la seguente formula strutturale:
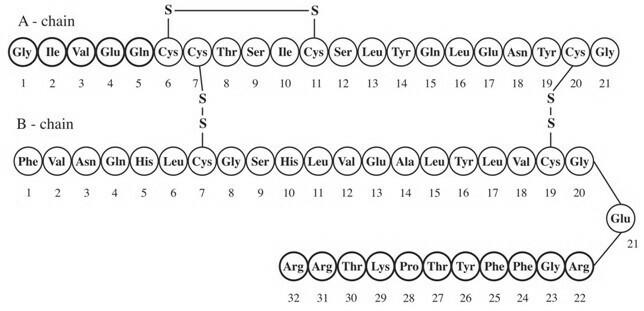
Lantus è costituito da insulina glargine disciolta in un fluido acquoso trasparente. Ogni millilitro di Lantus (iniezione di insulina glargine) contiene 100 UI (3,6378 mg) di insulina glargine.
Gli ingredienti inattivi per il flaconcino da 10 ml sono 30 mcg di zinco, 2,7 mg di m-cresolo, 20 mg di glicerolo 85%, 20 mcg di polisorbato 20 e acqua per preparazioni iniettabili.
Gli ingredienti inattivi per la cartuccia da 3 mL sono 30 mcg di zinco, 2,7 mg di m-cresolo, 20 mg di glicerolo all'85% e acqua per preparazioni iniettabili.
Il pH viene regolato mediante aggiunta di soluzioni acquose di acido cloridrico e idrossido di sodio. Lantus ha un pH di circa 4.
superiore
Farmacologia clinica
Meccanismo di azione
L'attività primaria dell'insulina, compresa l'insulina glargine, è la regolazione del metabolismo del glucosio. L'insulina e i suoi analoghi abbassano i livelli di glucosio nel sangue stimolando l'assorbimento periferico di glucosio, specialmente da parte dei muscoli scheletrici e dei grassi, e inibendo la produzione di glucosio epatico. L'insulina inibisce la lipolisi nell'adipocita, inibisce la proteolisi e migliora la sintesi proteica.
farmacodinamica
L'insulina glargine è un analogo dell'insulina umana progettato per avere una bassa solubilità acquosa a pH neutro. A pH 4, come nella soluzione di iniezione di Lantus, è completamente solubile. Dopo l'iniezione nel tessuto sottocutaneo, la soluzione acida viene neutralizzata, portando alla formazione di microprecipitati da cui piccoli quantità di insulina glargine vengono rilasciate lentamente, determinando un profilo di concentrazione / tempo relativamente costante per 24 ore senza pronunciato picco. Questo profilo consente il dosaggio una volta al giorno come insulina basale del paziente.
Negli studi clinici, l'effetto ipoglicemizzante su base molare (cioè somministrato alle stesse dosi) di insulina glargine per via endovenosa è approssimativamente lo stesso dell'insulina umana. Negli studi sul clamp euglicemico in soggetti sani o in pazienti con diabete di tipo 1, l'insorgenza dell'azione dell'insulina glargine sottocutanea è stata più lenta dell'insulina umana NPH. Il profilo dell'effetto dell'insulina glargine era relativamente costante senza picco pronunciato e la durata del suo effetto era prolungata rispetto all'insulina umana NPH. La Figura 1 mostra i risultati di uno studio condotto su pazienti con diabete di tipo 1 condotto per un massimo di 24 ore dopo l'iniezione. Il tempo mediano tra l'iniezione e la fine dell'effetto farmacologico è stato di 14,5 ore (intervallo: 9,5-19,3 ore) per NPH insulina umana e 24 ore (intervallo: da 10,8 a> 24,0 ore) (24 ore era la fine del periodo di osservazione) per l'insulina glargine.
Figura 1. Profilo di attività nei pazienti con diabete di tipo 1 ”
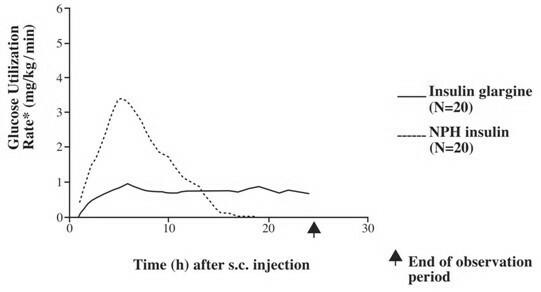
* Determinato come quantità di glucosio infuso per mantenere livelli di glucosio plasmatici costanti (valori medi orari); indicativo dell'attività dell'insulina.
â € Variabilità tra pazienti (CV, coefficiente di variazione); insulina glargine, 84% e NPH, 78%.
La maggiore durata d'azione (fino a 24 ore) di Lantus è direttamente correlata al suo più lento tasso di assorbimento e supporta la somministrazione sottocutanea una volta al giorno. Il corso dell'azione delle insuline, incluso Lantus, può variare tra individui e / o all'interno dello stesso individuo.
farmacocinetica
Assorbimento e biodisponibilità
Dopo l'iniezione sottocutanea di insulina glargine in soggetti sani e in pazienti diabetici, le concentrazioni sieriche di insulina hanno indicato un assorbimento più lento, più prolungato e un profilo di concentrazione / tempo relativamente costante per 24 ore senza picco pronunciato rispetto all'NPH umano insulina. Le concentrazioni sieriche di insulina erano quindi coerenti con il profilo temporale dell'attività farmacodinamica dell'insulina glargine.
Dopo l'iniezione sottocutanea di 0,3 UI / kg di insulina glargine in pazienti con diabete di tipo 1, è stato dimostrato un profilo concentrazione / tempo relativamente costante. La durata dell'azione dopo la somministrazione sottocutanea addominale, deltoidea o della coscia era simile.
Metabolismo
Uno studio sul metabolismo nell'uomo indica che l'insulina glargine è parzialmente metabolizzata nel terminale carbossilico della catena B nel sottocutaneo deposito per formare due metaboliti attivi con attività in vitro simile a quella dell'insulina, M1 (21A-Gly-insulina) e M2 (21A-Gly-des-30B-Thr-insulina). Nella circolazione sono presenti anche farmaci immodificati e questi prodotti di degradazione.
Popolazioni speciali
Età, razza e genere
Non sono disponibili informazioni sugli effetti dell'età, della razza e del sesso sulla farmacocinetica di Lantus. Tuttavia, in studi clinici controllati su adulti (n = 3890) e uno studio clinico controllato su pazienti pediatrici (n = 349), sottogruppo le analisi basate su età, razza e sesso non hanno mostrato differenze nella sicurezza e nell'efficacia tra insulina glargine e NPH umana insulina.
fumo
L'effetto del fumo sulla farmacocinetica / farmacodinamica di Lantus non è stato studiato.
Gravidanza
L'effetto della gravidanza sulla farmacocinetica e farmacodinamica di Lantus non è stato studiato (vedere PRECAUZIONI, Gravidanza).
Obesità
In studi clinici controllati, che includevano pazienti con indice di massa corporea (BMI) fino a 49,6 kg / m2 inclusi, le analisi dei sottogruppi basate su BMI non hanno mostrato differenze nella sicurezza e nell'efficacia tra insulina glargine e NPH umana insulina.
Insufficienza renale
L'effetto della compromissione renale sulla farmacocinetica di Lantus non è stato studiato. Tuttavia, alcuni studi con insulina umana hanno mostrato livelli aumentati di insulina circolante in pazienti con insufficienza renale. Può essere necessario un attento monitoraggio del glucosio e aggiustamenti della dose di insulina, incluso Lantus, nei pazienti con disfunzione renale (vedere PRECAUZIONI, Insufficienza renale).
Insufficienza epatica
L'effetto della compromissione epatica sulla farmacocinetica di Lantus non è stato studiato. Tuttavia, alcuni studi con insulina umana hanno mostrato livelli aumentati di insulina circolante in pazienti con insufficienza epatica. Può essere necessario un attento monitoraggio del glucosio e aggiustamenti della dose di insulina, incluso Lantus, in pazienti con disfunzione epatica (vedere PRECAUZIONI, Insufficienza epatica).
Studi clinici
La sicurezza e l'efficacia dell'insulina glargine somministrate una volta al giorno prima di coricarsi sono state confrontate con quelle dell'insulina umana NPH una volta al giorno e due volte al giorno in aperto, randomizzati, studi paralleli a controllo attivo su 2327 pazienti adulti e 349 pazienti pediatrici con diabete mellito di tipo 1 e 1563 pazienti adulti con diabete mellito di tipo 2 (vedere tabelle 1-3). In generale, la riduzione dell'emoglobina glicata (HbA1c) con Lantus era simile a quella dell'insulina umana NPH. I tassi complessivi di ipoglicemia non differivano tra i pazienti con diabete trattati con Lantus rispetto all'insulina umana NPH.
Diabete di tipo 1 per adulti (vedere la tabella 1).
In due grandi studi clinici randomizzati e controllati (Studi A e B), pazienti con diabete di tipo 1 (Studio A; n = 585, studio B; n = 534) sono stati randomizzati al trattamento in bolo basale con Lantus una volta al giorno prima di coricarsi o all'insulina umana NPH una o due volte al giorno e trattati per 28 settimane. L'insulina umana regolare è stata somministrata prima di ogni pasto. Lantus è stato somministrato prima di coricarsi. L'insulina umana NPH è stata somministrata una volta al giorno prima di coricarsi o al mattino e prima di coricarsi se usata due volte al giorno. In uno studio clinico controllato randomizzato di grandi dimensioni (studio C), pazienti con diabete di tipo 1 (n = 619) sono stati trattati per 16 settimane con un regime di insulina in bolo basale in cui è stata utilizzata l'insulina lispro prima di ciascuno pasto. Lantus è stato somministrato una volta al giorno prima di coricarsi e l'insulina umana NPH è stata somministrata una o due volte al giorno. In questi studi, l'insulina umana Lantus e NPH ha avuto un effetto simile sulla glicoemoglobina con un tasso complessivo simile di ipoglicemia.
Tabella 1: diabete mellito di tipo 1-adulto
| Studio A | Studio B | Studio C | ||||
|---|---|---|---|---|---|---|
| Durata del trattamento | 28 settimane | 28 settimane | 16 settimane | |||
| Trattamento in combinazione con | Insulina regolare | Insulina regolare | Insulina lispro | |||
| Lantus | NPH | Lantus | NPH | Lantus | NPH | |
| Numero di soggetti trattati | 292 | 293 | 264 | 270 | 310 | 309 |
| HbA1c | ||||||
| Endstudy significa | 8.13 | 8.07 | 7.55 | 7.49 | 7.53 | 7.60 |
| Adj. variazione media rispetto al basale | +0.21 | +0.10 | -0.16 | -0.21 | -0.07 | -0.08 |
| Lantus - NPH | +0.11 | +0.05 | +0.01 | |||
| IC al 95% per differenza di trattamento | (-0.03; +0.24) | (-0.08; +0.19) | (-0.11; +0.13) | |||
| Dose di insulina basale | ||||||
| Endstudy significa | 19.2 | 22.8 | 24.8 | 31.3 | 23.9 | 29.2 |
| Variazione media rispetto al basale | -1.7 | -0.3 | -4.1 | +1.8 | -4.5 | +0.9 |
| Dose totale di insulina | ||||||
| Endstudy significa | 46.7 | 51.7 | 50.3 | 54.8 | 47.4 | 50.7 |
| Variazione media rispetto al basale | -1.1 | -0.1 | +0.3 | +3.7 | -2.9 | +0.3 |
| Glicemia a digiuno (mg / dL) | ||||||
| Endstudy significa | 146.3 | 150.8 | 147.8 | 154.4 | 144.4 | 161.3 |
| Adj. variazione media rispetto al basale | -21.1 | -16.0 | -20.2 | -16.9 | -29.3 | -11.9 |
Diabete di tipo 1 pediatrico (vedere la tabella 2).
In uno studio clinico randomizzato e controllato (Studio D), pazienti pediatrici (età compresa tra 6 e 15 anni) con diabete di tipo 1 (n = 349) sono stati trattati per 28 settimane con un regime di insulina in bolo basale in cui è stata utilizzata l'insulina umana regolare prima di pasto. Lantus è stato somministrato una volta al giorno prima di coricarsi e l'insulina umana NPH è stata somministrata una o due volte al giorno. In entrambi i gruppi di trattamento sono stati osservati effetti simili sulla glicemoglobina e sull'incidenza dell'ipoglicemia.
Tabella 2: diabete mellito di tipo 1 pediatrico
| Studio D | ||
|---|---|---|
| Durata del trattamento | 28 settimane | |
| Trattamento in combinazione con | Insulina regolare | |
| Lantus | NPH | |
| Numero di soggetti trattati | 174 | 175 |
| HbA1c | ||
| Endstudy significa | 8.91 | 9.18 |
| Adj. variazione media rispetto al basale | +0.28 | +0.27 |
| Lantus - NPH | +0.01 | |
| IC al 95% per differenza di trattamento | (-0.24; +0.26) | |
| Dose di insulina basale | ||
| Endstudy significa | 18.2 | 21.1 |
| Variazione media rispetto al basale | -1.3 | +2.4 |
| Dose totale di insulina | ||
| Endstudy significa | 45.0 | 46.0 |
| Variazione media rispetto al basale | +1.9 | +3.4 |
| Glicemia a digiuno (mg / dL) | ||
| Endstudy significa | 171.9 | 182.7 |
| Adj. variazione media rispetto al basale | -23.2 | -12.2 |
Diabete di tipo 2 per adulti (vedere la tabella 3).
In un ampio studio clinico randomizzato e controllato (Studio E) (n = 570), Lantus è stato valutato per 52 settimane nell'ambito di un regime di terapia di combinazione con insulina e agenti antidiabetici orali (una sulfonilurea, metformina, acarbosio o combinazioni di questi farmaci). Lantus somministrato una volta al giorno prima di coricarsi è risultato efficace quanto l'insulina umana NPH somministrata una volta al giorno prima di coricarsi nel ridurre la glicemia e la glicemia a digiuno. C'era un basso tasso di ipoglicemia simile nei pazienti trattati con insulina umana Lantus e NPH. In un ampio studio clinico randomizzato e controllato (Studio F), in pazienti con diabete di tipo 2 che non usano agenti antidiabetici orali (n = 518), è stato valutato un regime di bolo basale di Lantus una volta al giorno prima di coricarsi o l'insulina umana NPH somministrata una o due volte al giorno 28 settimane Insulina umana regolare è stata utilizzata prima dei pasti, se necessario. Lantus ha mostrato un'efficacia simile a quella dell'insulina umana NPH una o due volte al giorno nel ridurre la glicemoglobina e il glucosio a digiuno con un'incidenza simile di ipoglicemia.
Tabella 3: diabete mellito di tipo 2-adulto
| Studio E | Studio F | |||
|---|---|---|---|---|
| Durata del trattamento | 52 settimane | 28 settimane | ||
| Trattamento in combinazione con | Agenti orali | Insulina regolare | ||
| Lantus | NPH | Lantus | NPH | |
| Numero di soggetti trattati | 289 | 281 | 259 | 259 |
| HbA1c | ||||
| Endstudy significa | 8.51 | 8.47 | 8.14 | 7.96 |
| Adj. variazione media rispetto al basale | -0.46 | -0.38 | -0.41 | -0.59 |
| Lantus - NPH | -0.08 | +0.17 | ||
| IC al 95% per differenza di trattamento | (-0.28; +0.12) | (-0.00; +0.35) | ||
| Dose di insulina basale | ||||
| Endstudy significa | 25.9 | 23.6 | 42.9 | 52.5 |
| Variazione media rispetto al basale | +11.5 | +9.0 | -1.2 | +7.0 |
| Dose totale di insulina | ||||
| Endstudy significa | 25.9 | 23.6 | 74.3 | 80.0 |
| Variazione media rispetto al basale | +11.5 | +9.0 | +10.0 | +13.1 |
| Glicemia a digiuno (mg / dL) | ||||
| Endstudy significa | 126.9 | 129.4 | 141.5 | 144.5 |
| Adj. variazione media rispetto al basale | -49.0 | -46.3 | -23.8 | -21.6 |
Dosaggio giornaliero flessibile Lantus
La sicurezza e l'efficacia di Lantus somministrate prima di colazione, prima di cena o prima di coricarsi erano valutato in uno studio clinico ampio, randomizzato e controllato, in pazienti con diabete di tipo 1 (studio G, n = 378). I pazienti sono stati anche trattati con insulina lispro durante i pasti. Lantus somministrato in diversi momenti della giornata ha portato a riduzioni simili dell'emoglobina glicata rispetto a quella con la somministrazione prima di coricarsi (vedere la Tabella 4). In questi pazienti, i dati sono disponibili dal monitoraggio del glucosio domiciliare a 8 punti. Il livello medio massimo di glucosio nel sangue è stato osservato appena prima dell'iniezione di Lantus indipendentemente dal momento della somministrazione, vale a dire prima di colazione, prima di cena o prima di coricarsi.
In questo studio, il 5% dei pazienti nel braccio Lantus-colazione ha sospeso il trattamento a causa della mancanza di efficacia. Nessun paziente negli altri due bracci ha sospeso per questo motivo. Il monitoraggio di routine durante questo studio ha rivelato i seguenti cambiamenti medi della pressione arteriosa sistolica: gruppo pre-colazione, 1,9 mm Hg; gruppo pre-cena, 0,7 mm Hg; gruppo prima di coricarsi, -2,0 mm Hg.
Anche la sicurezza e l'efficacia di Lantus somministrate prima della colazione o prima di coricarsi sono state valutate in modo ampio, randomizzato, studio clinico a controllo attivo (Studio H, n = 697) in pazienti con diabete di tipo 2 non più adeguatamente controllati con l'agente orale terapia. Tutti i pazienti in questo studio hanno anche ricevuto 3 mg di AMARYL® (glimepiride) al giorno. Lantus somministrato prima di colazione è stato altrettanto efficace nel ridurre l'emoglobina glicata A1c (HbA1c) rispetto a Lantus somministrato prima di coricarsi o insulina umana NPH somministrata prima di coricarsi (vedere Tabella 4).
Tabella 4: Dosaggio giornaliero flessibile di Lantus nel diabete mellito di tipo 1 (studio G) e di tipo 2 (studio H)
| Studio G | Studio H | |||||
|---|---|---|---|---|---|---|
| Treatmentduration | 24 settimane | 24 settimane | ||||
| Trattamento in combinazione con: | Insulina lispro | AMARYL® (glimepiride) | ||||
| Lantus Prima colazione |
Lantus Cena |
Lantus Bedtime |
Lantus Prima colazione |
Lantus Bedtime |
NPH Bedtime |
|
| ||||||
| Numero di soggetti trattati* | 112 | 124 | 128 | 234 | 226 | 227 |
| HbA1c | ||||||
| Media di base | 7.56 | 7.53 | 7.61 | 9.13 | 9.07 | 9.09 |
| Endstudy significa | 7.39 | 7.42 | 7.57 | 7.87 | 8.12 | 8.27 |
| Variazione media rispetto al basale | -0.17 | -0.11 | -0.04 | -1.26 | -0.95 | -0.83 |
| Dose basale di insulina (UI) | ||||||
| Endstudy significa | 27.3 | 24.6 | 22.8 | 40.4 | 38.5 | 36.8 |
| Variazione media rispetto al basale | 5.0 | 1.8 | 1.5 | |||
| Dose totale di insulina (UI) | Naa € | N / A | N / A | |||
| Endstudy significa | 53.3 | 54.7 | 51.5 | |||
| Variazione media rispetto al basale | 1.6 | 3.0 | 2.3 |
superiore
Indicazioni e utilizzo
Lantus è indicato per la somministrazione sottocutanea una volta al giorno per il trattamento di pazienti adulti e pediatrici di tipo 1 diabete mellito o pazienti adulti con diabete mellito di tipo 2 che richiedono insulina basale (a lunga durata d'azione) per il controllo di iperglicemia.
superiore
Controindicazioni
Lantus è controindicato nei pazienti ipersensibili all'insulina glargine o agli eccipienti.
superiore
Avvertenze
L'ipoglicemia è l'effetto avverso più comune dell'insulina, incluso Lantus. Come con tutte le insuline, i tempi dell'ipoglicemia possono differire tra le varie formulazioni di insulina. Il monitoraggio del glucosio è raccomandato per tutti i pazienti con diabete.
Qualsiasi cambiamento di insulina deve essere effettuato con cautela e solo sotto controllo medico. Cambiamenti nella concentrazione di insulina, tempistica del dosaggio, produttore, tipo (ad es. Analoghi regolari, NPH o insulina), specie (animale, umano) o metodo di fabbricazione (DNA ricombinante rispetto all'insulina animale) può comportare la necessità di un cambiamento dosaggio. Potrebbe essere necessario modificare il trattamento concomitante con antidiabetici orali.
superiore
Precauzioni
Generale
Lantus non è destinato alla somministrazione endovenosa. La durata prolungata dell'attività dell'insulina glargine dipende dall'iniezione nel tessuto sottocutaneo. La somministrazione endovenosa della consueta dose sottocutanea può provocare grave ipoglicemia.
Lantus NON deve essere diluito o miscelato con qualsiasi altra insulina o soluzione. Se Lantus viene diluito o miscelato, la soluzione può diventare torbida e il profilo farmacocinetico / farmacodinamico (ad es. inizio d'azione, tempo al picco dell'effetto) di Lantus e / o l'insulina mista possono essere alterati in modo imprevedibile maniera. Quando Lantus e l'insulina umana regolare sono stati miscelati immediatamente prima dell'iniezione nei cani, è stata osservata una ritardata insorgenza d'azione e il tempo al massimo effetto per l'insulina umana regolare. Anche la biodisponibilità totale della miscela è stata leggermente ridotta rispetto alle iniezioni separate di Lantus e insulina umana regolare. La rilevanza di queste osservazioni nei cani per l'uomo non è nota.
Come con tutte le preparazioni di insulina, il corso temporale dell'azione di Lantus può variare in soggetti diversi o in modo diverso volte nello stesso individuo e il tasso di assorbimento dipende dall'afflusso di sangue, dalla temperatura e dal fisico attività.
L'insulina può causare ritenzione di sodio ed edema, in particolare se un controllo metabolico precedentemente scarso è migliorato dall'intensificazione della terapia insulinica.
L'ipoglicemia
Come con tutti i preparati di insulina, le reazioni ipoglicemizzanti possono essere associate alla somministrazione di Lantus. L'ipoglicemia è l'effetto avverso più comune delle insuline. I sintomi di allarme precoce dell'ipoglicemia possono essere diversi o meno pronunciati in determinate condizioni, come ad es durata del diabete, malattie dei nervi diabetici, uso di farmaci come i beta-bloccanti o controllo intensivo del diabete (vedere PRECAUZIONI, Interazioni farmacologiche). Tali situazioni possono causare grave ipoglicemia (e, possibilmente, perdita di coscienza) prima della consapevolezza dei pazienti dell'ipoglicemia.
Il tempo di insorgenza dell'ipoglicemia dipende dal profilo d'azione delle insuline utilizzate e può, pertanto, cambiare quando viene modificato il regime di trattamento o i tempi di somministrazione. I pazienti che passano dall'insulina NPH due volte al giorno a Lantus una volta al giorno dovrebbero avere la loro iniziale La dose di Lantus è stata ridotta del 20% rispetto alla precedente dose totale giornaliera di NPH per ridurre il rischio di ipoglicemia (vedere DOSAGGIO E SOMMINISTRAZIONE, Passaggio a Lantus).
L'effetto prolungato di Lantus sottocutaneo può ritardare il recupero dall'ipoglicemia.
In uno studio clinico, i sintomi dell'ipoglicemia o le risposte dell'ormone controregolatore erano simili dopo insulina glargine per via endovenosa e insulina umana regolare sia in soggetti sani che in pazienti di tipo 1 diabete.
Insufficienza renale
Sebbene non siano stati condotti studi su pazienti con diabete e insufficienza renale, i requisiti di Lantus può essere ridotto a causa del ridotto metabolismo dell'insulina, simile alle osservazioni riscontrate con altre insuline (vedere FARMACOLOGIA CLINICA, Popolazioni speciali).
Insufficienza epatica
Sebbene non siano stati condotti studi su pazienti con diabete e insufficienza epatica, i requisiti di Lantus possono essere ridotti a causa della ridotta capacità di gluconeogenesi e del ridotto metabolismo dell'insulina, simile alle osservazioni riscontrate con altre insuline (vedere FARMACOLOGIA CLINICA, Popolazioni speciali).
Sito di iniezione e reazioni allergiche
Come con qualsiasi terapia insulinica, la lipodistrofia può verificarsi nel sito di iniezione e ritardare l'assorbimento dell'insulina. Altre reazioni al sito di iniezione con terapia insulinica comprendono arrossamento, dolore, prurito, orticaria, gonfiore e infiammazione. La rotazione continua del sito di iniezione all'interno di una determinata area può aiutare a ridurre o prevenire queste reazioni. La maggior parte delle reazioni minori alle insuline di solito si risolvono in pochi giorni o alcune settimane.
Le segnalazioni di dolore al sito di iniezione sono state più frequenti con l'insulina umana Nant rispetto a NPH (2,7% di insulina glargine contro 0,7% di NPH). Le segnalazioni di dolore nel sito di iniezione erano generalmente lievi e non hanno comportato l'interruzione della terapia.
Le reazioni allergiche di tipo immediato sono rare. Tali reazioni all'insulina (inclusa l'insulina glargine) o agli eccipienti possono, ad esempio, essere associate con reazioni cutanee generalizzate, angioedema, broncospasmo, ipotensione o shock e può essere la vita minaccioso.
Condizioni intercorrenti
Il fabbisogno di insulina può essere modificato durante condizioni intercorrenti come malattia, disturbi emotivi o stress.
Informazioni per i pazienti
Lantus deve essere usato solo se la soluzione è limpida e incolore senza particelle visibili (vedi DOSAGGIO E SOMMINISTRAZIONE, Preparazione e trattamento).
I pazienti devono essere informati che Lantus NON deve essere diluito o miscelato con qualsiasi altra insulina o soluzione (vedere PRECAUZIONI, Generale).
I pazienti devono essere istruiti sulle procedure di autogestione tra cui il monitoraggio del glucosio, la corretta tecnica di iniezione e la gestione dell'ipoglicemia e dell'iperglicemia. I pazienti devono essere istruiti sulla gestione di situazioni speciali come condizioni intercorrenti (malattia, stress o emotivo) disturbi), una dose di insulina inadeguata o saltata, la somministrazione involontaria di una dose di insulina aumentata, l'assunzione di cibo inadeguata, o pasti saltati. Riferire i pazienti alla circolare "Informazioni paziente" di Lantus per ulteriori informazioni.
Come per tutti i pazienti con diabete, la capacità di concentrazione e / o di reazione può essere compromessa a causa di ipoglicemia o iperglicemia.
I pazienti con diabete dovrebbero essere informati di informare il proprio medico se sono in gravidanza o stanno prendendo in considerazione una gravidanza.
Interazioni farmacologiche
Numerose sostanze influenzano il metabolismo del glucosio e possono richiedere un aggiustamento della dose di insulina e un monitoraggio particolarmente attento.
I seguenti sono esempi di sostanze che possono aumentare l'effetto ipoglicemizzante e la suscettibilità all'ipoglicemia: prodotti antidiabetici orali, ACE-inibitori, disopiramide, fibrati, fluoxetina, inibitori MAO, propossifene, salicilati, analogo della somatostatina (ad es. Octreotide), sulfonamide antibiotici.
I seguenti sono esempi di sostanze che possono ridurre l'effetto ipoglicemizzante dell'insulina: corticosteroidi, danazolo, diuretici, agenti simpaticomimetici (ad es. epinefrina, albuterolo, terbutalina), isoniazide, derivati della fenotiazina, somatropina, ormoni tiroidei, estrogeni, progestinici (ad es. nei contraccettivi orali), inibitori della proteasi e farmaci antipsicotici atipici (ad es. olanzapina e clozapina).
I beta-bloccanti, la clonidina, i sali di litio e l'alcol possono potenziare o indebolire l'effetto ipoglicemizzante dell'insulina. La pentamidina può causare ipoglicemia, che a volte può essere seguita da iperglicemia.
Inoltre, sotto l'influenza di medicinali simpatici, come i beta-bloccanti, la clonidina, la guanetidina e la reserpina, i segni di ipoglicemia possono essere ridotti o assenti.
Cancerogenesi, mutagenesi, alterazione della fertilità
Nei topi e nei ratti, sono stati condotti studi standard di carcinogenicità a due anni con insulina glargine a dosi fino a 0,455 mg / kg, che è per il ratto circa 10 volte e per il mouse circa 5 volte la dose iniziale sottocutanea raccomandata nell'uomo di 10 UI (0,008 mg / kg / giorno), in base a mg / m2. I risultati nei topi femmine non sono stati conclusivi a causa dell'eccessiva mortalità in tutti i gruppi di dosaggio durante lo studio. Gli istiocitomi sono stati trovati nei siti di iniezione nei ratti maschi (statisticamente significativi) e nei topi maschi (non statisticamente significativi) in gruppi contenenti veicoli acidi. Questi tumori non sono stati trovati negli animali di sesso femminile, nel controllo della soluzione salina o nei gruppi di confronto dell'insulina usando un veicolo diverso. La rilevanza di questi risultati per l'uomo non è nota.
L'insulina glargine non è risultata mutagena nei test per la rilevazione di mutazioni geniche in batteri e cellule di mammifero (Ames- e Test HGPRT) e nei test per la rilevazione di aberrazioni cromosomiche (citogenetica in vitro nelle cellule V79 e in vivo in cinese criceti).
In uno studio combinato sulla fertilità e prenatale e postnatale in ratti maschi e femmine a dosi sottocutanee fino a 0,36 mg / kg / die, che è circa 7 volte il la dose iniziale raccomandata sottocutanea nell'uomo di 10 UI (0,008 mg / kg / die), basata su mg / m2, tossicità materna dovuta a ipoglicemia dose-dipendente, inclusi alcuni decessi, era osservato. Di conseguenza, una riduzione del tasso di allevamento si è verificata solo nel gruppo ad alte dosi. Effetti simili sono stati osservati con insulina umana NPH.
Gravidanza
Effetti teratogeni
Categoria di gravidanza C. Sono stati condotti studi sottocutanei di riproduzione e teratologia con insulina glargine e insulina umana regolare nei ratti e nei conigli dell'Himalaya. Il farmaco è stato somministrato alle femmine di ratto prima dell'accoppiamento, durante l'accoppiamento e durante la gravidanza a dosi fino a 0,36 mg / kg / giorno, che è circa 7 volte la dose iniziale sottocutanea raccomandata nell'uomo di 10 UI (0,008 mg / kg / giorno), in base a mg / m2. Nei conigli, dosi di 0,072 mg / kg / die, pari a circa 2 volte l'uomo raccomandato una dose iniziale sottocutanea di 10 UI (0,008 mg / kg / giorno), basata su mg / m2, è stata somministrata durante organogenesi. Gli effetti dell'insulina glargine non differivano generalmente da quelli osservati con insulina umana normale nei ratti o nei conigli. Tuttavia, nei conigli, cinque feti di due cucciolate del gruppo ad alto dosaggio hanno mostrato dilatazione dei ventricoli cerebrali. Fertilità e sviluppo embrionale precoce sembravano normali.
Non esistono studi clinici ben controllati sull'uso dell'insulina glargine in donne in gravidanza. È essenziale per i pazienti con diabete o con una storia di diabete gestazionale mantenere un buon controllo metabolico prima del concepimento e durante la gravidanza. Il fabbisogno di insulina può diminuire durante il primo trimestre, generalmente aumentare durante il secondo e il terzo trimestre e diminuire rapidamente dopo il parto. In questi pazienti è essenziale un attento monitoraggio del controllo del glucosio. Poiché gli studi sulla riproduzione animale non sono sempre predittivi della risposta umana, questo farmaco deve essere usato durante la gravidanza solo se chiaramente necessario.
Madri che allattano
Non è noto se l'insulina glargine sia escreta in quantità significative nel latte materno. Molti farmaci, compresa l'insulina umana, vengono escreti nel latte materno. Per questo motivo, si deve usare cautela quando Lantus viene somministrato a una donna che allatta. Le donne che allattano possono richiedere aggiustamenti della dose di insulina e della dieta.
Uso pediatrico
La sicurezza e l'efficacia di Lantus sono state stabilite nella fascia di età da 6 a 15 anni con diabete di tipo 1.
Uso geriatrico
In studi clinici controllati che hanno confrontato l'insulina glargine con l'insulina umana NPH, 593 su 3890 pazienti con diabete di tipo 1 e di tipo 2 avevano 65 anni e più. L'unica differenza di sicurezza o efficacia in questa sottopopolazione era rispetto all'intera popolazione di studio un'incidenza più alta attesa di eventi cardiovascolari sia nell'insulina glargine sia nell'NPH trattata con insulina umana pazienti.
Nei pazienti anziani con diabete, la dose iniziale, gli incrementi della dose e il dosaggio di mantenimento devono essere conservativi per evitare reazioni ipoglicemizzanti. L'ipoglicemia può essere difficile da riconoscere negli anziani (vedi PRECAUZIONI, Ipoglicemia).
superiore
Reazioni avverse
Gli eventi avversi comunemente associati a Lantus includono:
Corpo nel suo insieme: reazioni allergiche (vedi PRECAUZIONI).
Pelle e appendici: reazione nel sito di iniezione, lipodistrofia, prurito, eruzione cutanea (vedi PRECAUZIONI).
Altro: ipoglicemia (vedi AVVERTENZE e PRECAUZIONI).
Negli studi clinici condotti su pazienti adulti, si è verificata una maggiore incidenza di dolore nel sito di iniezione emergente dal trattamento nei pazienti trattati con Lantus (2,7%) rispetto ai pazienti trattati con insulina NPH (0,7%). Le segnalazioni di dolore nel sito di iniezione erano generalmente lievi e non hanno comportato l'interruzione della terapia. Altre reazioni al sito di iniezione emergenti dal trattamento si sono verificate in casi simili con insulina glargine e insulina umana NPH.
La retinopatia è stata valutata negli studi clinici mediante eventi avversi retinici segnalati e fotografia del fondo. Il numero di eventi avversi della retina riportati per i gruppi di trattamento con Lantus e NPH era simile per i pazienti con diabete di tipo 1 e di tipo 2. La progressione della retinopatia è stata studiata dalla fotografia del fondo utilizzando un protocollo di classificazione derivato dallo studio sulla retinopatia diabetica a trattamento precoce (ETDRS). In uno studio clinico su pazienti con diabete di tipo 2, una differenza nel numero di soggetti con 3 fasi la progressione della scala ETDRS su un periodo di 6 mesi è stata rilevata dalla fotografia del fondo (7,5% nel gruppo Lantus contro 2,7% nell'NPH gruppo trattato). La rilevanza complessiva di questo risultato isolato non può essere determinata a causa del numero limitato di pazienti coinvolti, il breve periodo di follow-up e il fatto che questo risultato non è stato osservato in altri studi clinici studi.
superiore
Overdose
Un eccesso di insulina rispetto all'assunzione di cibo, al dispendio energetico o ad entrambi può portare a ipoglicemia grave e talvolta a lungo termine e potenzialmente letale. Lievi episodi di ipoglicemia possono di solito essere trattati con carboidrati orali. Potrebbero essere necessari aggiustamenti del dosaggio del farmaco, dei modelli di pasto o dell'esercizio fisico.
Gli episodi più gravi con coma, convulsioni o danno neurologico possono essere trattati con glucagone intramuscolare / sottocutaneo o glucosio endovenoso concentrato. Dopo un evidente recupero clinico dall'ipoglicemia, possono essere necessarie l'osservazione continua e l'assunzione aggiuntiva di carboidrati per evitare il ripetersi di ipoglicemia.
superiore
Dosaggio e amministrazione
Lantus è un analogo dell'insulina umana ricombinante. La sua potenza è approssimativamente la stessa dell'insulina umana. Presenta un profilo ipoglicemizzante relativamente costante per 24 ore che consente il dosaggio una volta al giorno.
Lantus può essere somministrato in qualsiasi momento durante il giorno. Lantus deve essere somministrato per via sottocutanea una volta al giorno alla stessa ora ogni giorno. Per i pazienti che regolano i tempi di somministrazione del dosaggio con Lantus, vedere AVVERTENZE e PRECAUZIONI, Ipoglicemia. Lantus non è destinato alla somministrazione endovenosa (vedere PRECAUZIONI). La somministrazione endovenosa della consueta dose sottocutanea può provocare grave ipoglicemia. I livelli desiderati di glucosio nel sangue, nonché le dosi e i tempi dei farmaci antidiabetici devono essere determinati individualmente. Il monitoraggio della glicemia è raccomandato per tutti i pazienti con diabete. La durata prolungata dell'attività di Lantus dipende dall'iniezione nello spazio sottocutaneo.
Come per tutte le insuline, i siti di iniezione all'interno di un'area di iniezione (addome, coscia o deltoide) devono essere ruotati da un'iniezione all'altra.
Negli studi clinici, non vi è stata alcuna differenza rilevante nell'assorbimento di insulina glargine dopo somministrazione sottocutanea addominale, deltoide o della coscia. Come per tutte le insuline, il tasso di assorbimento, e di conseguenza l'inizio e la durata dell'azione, possono essere influenzati dall'esercizio e da altre variabili.
Lantus non è l'insulina di prima scelta per il trattamento del diabete chetoacidosi. Il trattamento preferito è l'insulina endovenosa a breve durata d'azione.
Uso pediatrico
Lantus può essere somministrato in sicurezza a pazienti pediatrici di età pari o inferiore a 6 anni. Somministrazione a pazienti pediatrici
Iniziazione della terapia Lantus
In uno studio clinico su pazienti con insulina naïve con diabete di tipo 2 già trattati con farmaci antidiabetici orali, Lantus è stato iniziato a una dose media di 10 UI una volta al giorno e successivamente aggiustata in base alle necessità del paziente su una dose giornaliera totale compresa tra 2 e 100 IU.
Passaggio a Lantus
Se si passa da un regime di trattamento con insulina ad azione intermedia o prolungata a un regime con Lantus, la quantità e la tempistica dell'insulina ad azione breve o dell'analogo dell'insulina ad azione rapida o la dose di qualsiasi farmaco antidiabetico orale può essere necessario aggiustato. Negli studi clinici, quando i pazienti sono stati trasferiti dall'insulina umana NPH una volta al giorno o dall'insulina umana ultralente al Lantus una volta al giorno, la dose iniziale di solito non è stata modificata. Tuttavia, quando i pazienti sono stati trasferiti dall'insulina umana NPH due volte al giorno a Lantus una volta al giorno, per ridurre il rischio di ipoglicemia, l'iniziale la dose (UI) è stata generalmente ridotta di circa il 20% (rispetto alla UI totale giornaliera di insulina umana NPH) e quindi aggiustata in base alla risposta del paziente (vedere PRECAUZIONI, Ipoglicemia).
Si raccomanda un programma di attento monitoraggio metabolico sotto controllo medico durante il trasferimento e nelle prime settimane successive. Potrebbe essere necessario regolare la quantità e i tempi dell'insulina ad azione breve o dell'analogo dell'insulina ad azione rapida. Ciò è particolarmente vero per i pazienti con anticorpi acquisiti contro l'insulina umana che necessitano di dosi elevate di insulina e si verifica con tutti gli analoghi dell'insulina. Potrebbe essere necessario un aggiustamento della dose di Lantus e altre insuline o farmaci antidiabetici orali; ad esempio, se si verificano i tempi di dosaggio, il peso o lo stile di vita del paziente o altre circostanze che aumentano la suscettibilità all'ipoglicemia o all'iperglicemia (vedere PRECAUZIONI, Ipoglicemia).
Potrebbe anche essere necessario modificare la dose durante la malattia intercorrente (vedere PRECAUZIONI, Condizioni intercorrenti).
Preparazione e gestione
I medicinali per uso parenterale devono essere ispezionati visivamente prima della somministrazione ogni volta che la soluzione e il contenitore lo consentono. Lantus deve essere usato solo se la soluzione è limpida e incolore senza particelle visibili.
Miscelazione e diluizione: Lantus NON deve essere diluito o miscelato con nessun'altra insulina o soluzione (vedere PRECAUZIONI, Generale).
Flaconcino: le siringhe non devono contenere altri medicinali o residui.
Sistema a cartuccia: se OptiClik®, il dispositivo di erogazione dell'insulina per Lantus, malfunzionamenti, Lantus può essere prelevato dal sistema a cartuccia in una siringa U-100 e iniettato.
superiore
Come viene fornito
Lantus 100 unità per ml (U-100) è disponibile nelle seguenti confezioni:
Flaconcini da 10 ml (NDC 0088-2220-33)
Sistema a cartuccia da 3 ml1, confezione da 5 (NDC 0088-2220-52)
1I sistemi a cartuccia devono essere utilizzati solo in OptiClik® (dispositivo per la somministrazione di insulina)
Conservazione
Sistema di fiala / cartuccia non aperto
I flaconcini e i sistemi di cartucce Lantus non aperti devono essere conservati in frigorifero, a una temperatura compresa tra 2 ° C e 8 ° C (36 ° F - 46 ° F). Lantus non deve essere conservato nel congelatore e non deve essere consentito il congelamento.
Scartare se è stato congelato.
Aprire il sistema (in uso) della fiala / cartuccia
Le fiale aperte, refrigerate o meno, devono essere utilizzate entro 28 giorni dal primo utilizzo. Devono essere eliminati se non utilizzati entro 28 giorni. Se la refrigerazione non è possibile, la fiala aperta può essere mantenuta non refrigerata per un massimo di 28 giorni lontano dal calore e dalla luce diretti, purché la temperatura non sia superiore a 30 ° C (86 ° F).
Il sistema di cartucce aperto (in uso) in OptiClik® NON deve essere refrigerato ma deve essere tenuto a temperatura ambiente (inferiore a 30 ° C) da fonti di calore e luce dirette. Il sistema di cartucce aperto (in uso) in OptiClik® mantenuto a temperatura ambiente deve essere eliminato dopo 28 giorni. Non conservare OptiClik®, con o senza sistema a cartuccia, in frigorifero in qualsiasi momento.
Lantus non deve essere conservato nel congelatore e non deve essere consentito il congelamento. Scartare se è stato congelato.
Queste condizioni di conservazione sono riassunte nella seguente tabella:
| Non in uso (Non aperto) refrigerato |
Non in uso (Non aperto) Temperatura ambiente |
In uso (ha aperto) (Vedi temperatura sotto) |
|
|---|---|---|---|
| Flaconcino da 10 ml | Fino alla data di scadenza | 28 giorni | 28 giorni Temperatura refrigerata o ambiente |
| Sistema a cartuccia da 3 ml | Fino alla data di scadenza | 28 giorni | 28 giorni Temperatura refrigerata o ambiente |
| Cartuccia da 3 ml sistema inserito in OptiClik® |
28 giorni Solo temperatura ambiente (Non refrigerare) |
Prodotto per un distribuito da:
sanofi-aventis U.S. LLC
Bridgewater NJ 08807
Fatto in Germania
www. Lantus.com
© 2006 sanofi-aventis U.S. LLC
OptiClik® è un marchio registrato di sanofi-aventis U.S. LLC, Bridgewater NJ 08807
ultimo aggiornamento 04/2006
Lantus, insulina glargine (origine di rDNA), informazioni per il paziente (in inglese semplice)
Informazioni dettagliate su segni, sintomi, cause, trattamenti del diabete
Le informazioni contenute in questa monografia non intendono coprire tutti i possibili usi, indicazioni, precauzioni, interazioni farmacologiche o effetti avversi. Questa informazione è generalizzata e non è intesa come consulenza medica specifica. Se ha domande sui medicinali che sta assumendo o desidera maggiori informazioni, consultare il medico, il farmacista o l'infermiere.
torna a: Sfoglia tutti i farmaci per il diabete



