Symlin per il trattamento del diabete
Marchio: Symlin, Symlin Pen
Nome generico: pramlintide acetato
Contenuti:
Descrizione
Farmacologia
Studi clinici
Indicazioni e utilizzo
Controindicazioni
Avvertenze
Precauzioni
Reazioni avverse
Overdose
Dosaggio e amministrazione
Come fornito
Conservazione
Symlin, Symlin Pen, pramlintide acetato, informazioni per il paziente (in un inglese semplice)
AVVERTIMENTO
Symlin è usato con insulina ed è stato associato ad un aumentato rischio di ipoglicemia grave indotta da insulina, in particolare nei pazienti con diabete di tipo 1. Quando si verifica una grave ipoglicemia associata all'uso di Symlin, si osserva entro 3 ore dall'iniezione di Symlin. Se si verifica una grave ipoglicemia durante la guida di un veicolo a motore, macchinari pesanti o durante altre attività ad alto rischio, possono verificarsi lesioni gravi. Una selezione appropriata del paziente, un'attenta istruzione del paziente e aggiustamenti della dose di insulina sono elementi critici per ridurre questo rischio.
Descrizione
L'iniezione di Symlin® (pramlintide acetato) è un farmaco antiiperglicemico da utilizzare in pazienti con diabete trattati con insulina. Pramlintide è un analogo sintetico dell'amilina umana, un ormone neuroendocrino presente in natura sintetizzato dalle cellule beta del pancreas che contribuisce al controllo del glucosio durante il periodo postprandiale. Pramlintide è fornito come sale acetato del polipeptide sintetico 37-aminoacido, che differisce nell'amminoacido sequenza acida dell'amilina umana mediante sostituzione con prolina nelle posizioni 25 (alanina), 28 (serina) e 29 (Serina).
La formula strutturale di pramlintide acetato è come mostrato:

Pramlintide acetato è una polvere bianca che ha una formula molecolare di C171H267N51O53S2- x C2H4O2 (3â ‰ ¤xâ ‰ ¤8); il peso molecolare è 3949,4. L'acetato di pramlintide è solubile in acqua.
Symlin è formulato come una soluzione chiara, isotonica e sterile per la somministrazione sottocutanea (SC). L'iniettore di penna monouso SymlinPen® multidose contiene 1000 mcg / mL di pramlintide (come acetato); I flaconcini di Symlin contengono 600 mcg / mL di pramlintide (come acetato). Entrambe le formulazioni contengono 2,25 mg / mL di metacresolo come conservante, D-mannitolo come modificatore di tonicità e acido acetico e acetato di sodio come modificatori del pH. Symlin ha un pH di circa 4,0.
superiore
Farmacologia clinica
Fisiologia dell'amilina
L'amilina è co-localizzata con insulina in granuli secretori e co-secreta con insulina da cellule beta del pancreas in risposta all'assunzione di cibo. Amilina e insulina mostrano simili modelli di digiuno e postprandiali in soggetti sani (Figura 1).
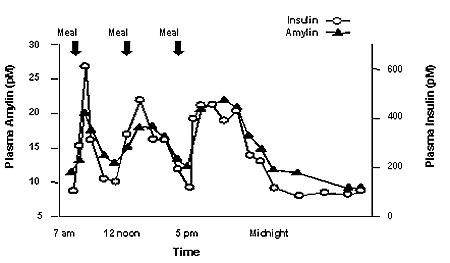
Figura 1: Profilo di secrezione di amilina e insulina in adulti sani
L'amilina influenza il tasso di comparsa del glucosio postprandiale attraverso una varietà di meccanismi. L'amilina rallenta lo svuotamento gastrico (cioè la velocità con cui il cibo viene rilasciato dallo stomaco all'intestino tenue) senza alterare l'assorbimento complessivo dei nutrienti. Inoltre, l'amilina sopprime la secrezione di glucagone (non normalizzata dalla sola insulina), che porta alla soppressione della produzione endogena di glucosio dal fegato. L'amilina regola anche l'assunzione di cibo a causa della modulazione dell'appetito mediata a livello centrale.
Nei pazienti con diabete di tipo 2 o di tipo 1 che utilizza insulina, le cellule beta del pancreas sono disfunzionali o danneggiate, con conseguente riduzione della secrezione di insulina e amilina in risposta al cibo.
Meccanismo di azione
Symlin, agendo come un agente amilinomimetico, ha i seguenti effetti: 1) modulazione dello svuotamento gastrico; 2) prevenzione dell'aumento postprandiale del glucagone plasmatico; e 3) sazietà che porta a una riduzione dell'apporto calorico e alla potenziale perdita di peso.
Svuotamento gastrico
Il tasso di svuotamento gastrico è un fattore determinante per l'aumento postprandiale del glucosio plasmatico. Symlin rallenta la velocità con cui il cibo viene rilasciato dallo stomaco all'intestino tenue dopo un pasto e, quindi, riduce l'aumento iniziale postprandiale del glucosio plasmatico. Questo effetto dura circa 3 ore dopo la somministrazione di Symlin. Symlin non altera l'assorbimento netto di carboidrati ingeriti o altri nutrienti.
Secrezione postprandiale di glucagone
Nei pazienti con diabete, le concentrazioni di glucagone sono anormalmente elevate durante il periodo postprandiale, contribuendo all'iperglicemia. Symlin ha dimostrato di ridurre le concentrazioni postprandiali di glucagone in pazienti diabetici che usano insulina.
Sazietà
Symlin somministrato prima di un pasto ha dimostrato di ridurre l'apporto calorico totale. Questo effetto sembra essere indipendente dalla nausea che può accompagnare il trattamento con Symlin.
farmacocinetica
Assorbimento
La biodisponibilità assoluta di una singola dose di SC di Symlin è approssimativamente dal 30 al 40%. La somministrazione sottocutanea di diverse dosi di Symlin nell'area addominale o nella coscia di soggetti sani ha determinato concentrazioni plasmatiche massime proporzionate alla dose (Cmax) e l'esposizione complessiva (espressa come area sotto la curva di concentrazione plasmatica o (AUC)) (Tabella 1).
Tabella 1: Parametri farmacocinetici medi a seguito della somministrazione di dosi singole di Symlin in SC
| SC Dose (Mcg) |
AUC (0-β) (Pmol * min / L) |
Cmax (Pmol / L) |
Tmax (Min) |
Eliminazione t ½ (Min) |
|---|---|---|---|---|
| 30 | 3750 | 39 | 21 | 55 |
| 60 | 6778 | 79 | 20 | 49 |
| 90 | 8507 | 102 | 19 | 51 |
| 120 | 11970 | 147 | 21 | 48 |
L'iniezione di Symlin nel braccio ha mostrato una maggiore esposizione con maggiore variabilità, rispetto all'esposizione dopo l'iniezione di Symlin nell'area addominale o nella coscia.
Non c'era una forte correlazione tra il grado di adiposità valutato dall'IMC o dalle misurazioni dello spessore della piega della pelle e la biodisponibilità relativa. Le iniezioni somministrate con aghi da 6,0 mm e 12,7 mm hanno prodotto una biodisponibilità simile.
Distribuzione
Symlin non si lega ampiamente alle cellule del sangue o all'albumina (circa il 40% del farmaco non è legato nel plasma), pertanto la farmacocinetica di Symlin dovrebbe essere insensibile ai cambiamenti nei siti di legame.
Metabolismo ed eliminazione
In soggetti sani, l'emivita di Symlin è di circa 48 minuti. Symlin è metabolizzato principalmente dai reni. Des-lys1 pramlintide (2-37 pramlintide), il metabolita primario, ha un'emivita simile ed è biologicamente attivo sia in vitro che in vivo nei ratti. I valori di AUC sono relativamente costanti con dosi ripetute, il che indica l'assenza di bioaccumulo.
Popolazioni speciali
Insufficienza renale
I pazienti con insufficienza renale moderata o grave (ClCr> 20 a â € ‰50 mL / min) non hanno mostrato un aumento dell'esposizione a Symlin o una riduzione della clearance di Symlin, rispetto ai soggetti con normale funzionalità renale. Non sono stati condotti studi su pazienti in dialisi.
Insufficienza epatica
Non sono stati condotti studi di farmacocinetica in pazienti con insufficienza epatica. Tuttavia, sulla base dell'elevato grado di metabolismo renale (vedere Metabolismo ed eliminazione), non si prevede che la disfunzione epatica influenzi le concentrazioni ematiche di Symlin.
geriatrico
Non sono stati condotti studi di farmacocinetica nella popolazione geriatrica. Symlin deve essere usato solo in pazienti noti per comprendere appieno e aderire ai corretti adeguamenti dell'insulina e al monitoraggio del glucosio. Non sono state osservate differenze coerenti con l'età nell'attività di Symlin nella popolazione geriatrica (n = 539 per pazienti di età pari o superiore a 65 anni negli studi clinici).
pediatrico
Symlin non è stato valutato nella popolazione pediatrica.
Genere
Nessuno studio è stato condotto per valutare i possibili effetti di genere sulla farmacocinetica di Symlin. Tuttavia, negli studi clinici non sono state osservate differenze coerenti tra i sessi nell'attività di Symlin (n = 2799 per i maschi e n = 2085 per le femmine).
Razza / etnia
Nessuno studio è stato condotto per valutare l'effetto dell'etnia sulla farmacocinetica di Symlin. Tuttavia, non sono state osservate differenze coerenti nell'attività di Symlin tra i pazienti di diversa razza / etnia negli studi clinici (n = 4257 per il bianco, n = 229 per il nero, n = 337 per ispanico e n = 61 per altri origini etniche).
Interazioni farmacologiche
L'effetto di Symlin (120 mcg) sulla farmacocinetica del paracetamolo (1000 mg) come marker di svuotamento gastrico è stato valutato in pazienti con diabete di tipo 2 (n = 24). Symlin non ha modificato in modo significativo l'AUC del paracetamolo. Tuttavia, Symlin ha ridotto il paracetamolo Cmax (circa il 29% con co-somministrazione simultanea) e aumentato il tempo alla massima concentrazione plasmatica o tmax (che varia da 48 a 72 minuti) in base al tempo di somministrazione del paracetamolo rispetto all'iniezione di Symlin. Symlin non ha influenzato significativamente il paracetamolo tmax quando il paracetamolo è stato somministrato da 1 a 2 ore prima dell'iniezione di Symlin. Tuttavia, la tmax di paracetamolo è stato significativamente aumentato quando il paracetamolo è stato somministrato contemporaneamente o fino a 2 ore dopo l'iniezione di Symlin (vedere PRECAUZIONI, Interazioni farmacologiche).
farmacodinamica
Negli studi clinici condotti su pazienti con diabete di tipo 2 e di tipo 1 a insulina, è risultata la somministrazione di Symlin in una riduzione delle concentrazioni medie postprandiali di glucosio, ridotte fluttuazioni di glucosio e riduzione degli alimenti assunzione. Le dosi di Symlin differiscono per i pazienti di tipo 2 e di tipo 1 che usano insulina (vedere DOSAGGIO E SOMMINISTRAZIONE).
Riduzione delle concentrazioni postprandiali di glucosio
Symlin somministrato per via sottocutanea immediatamente prima di un pasto ha ridotto le concentrazioni plasmatiche di glucosio dopo il pasto quando usato con insulina regolare o analoghi dell'insulina ad azione rapida (Figura 2). Questa riduzione del glucosio postprandiale ha ridotto la quantità di insulina a breve durata richiesta e ha limitato le fluttuazioni del glucosio in base al monitoraggio del glucosio nelle 24 ore. Quando venivano usate insuline analogiche ad azione rapida, le concentrazioni plasmatiche di glucosio tendevano ad aumentare durante l'intervallo tra 150 minuti dopo l'iniezione di Symlin e il pasto successivo (vedere DOSAGGIO E SOMMINISTRAZIONE).
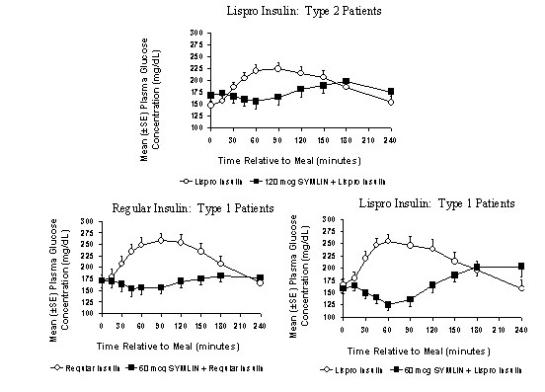
Figura 2: Profili postprandiali del glucosio plasmatico in pazienti con diabete di tipo 2 e di tipo 1 che ricevono Symlin e / o insulina
Assunzione di cibo ridotta
È stata associata una singola dose sottocutanea di Symlin 120 mcg (tipo 2) o 30 mcg (tipo 1) somministrata 1 ora prima di un pasto a buffet illimitato riduzioni dell'apporto calorico totale (variazioni medie sottratte dal placebo rispettivamente del ~ 23% e del 21%), che si sono verificate senza riduzioni del pasto durata.
superiore
Studi clinici
Un totale di 5325 pazienti e volontari sani hanno ricevuto Symlin negli studi clinici. Ciò include 1688 con diabete di tipo 2 e 2375 con diabete di tipo 1 in controllo a breve e lungo termine studi clinici, studi clinici incontrollati a lungo termine e uno studio in aperto nella pratica clinica ambientazione.
Studi clinici sul diabete di tipo 2
L'efficacia di una gamma di dosi di Symlin è stata valutata in numerosi studi clinici controllati verso placebo e in aperto su pazienti con diabete di tipo 2 che hanno usato insulina. Sulla base dei risultati ottenuti in questi studi, la dose raccomandata di Symlin per i pazienti con diabete di tipo 2 che utilizza insulina è di 120 mcg somministrati immediatamente prima dei pasti principali.
Sono stati condotti due studi a lungo termine (da 26 a 52 settimane), randomizzati, in doppio cieco, controllati con placebo su Symlin in pazienti con diabete di tipo 2 usando insulina a dose fissa per isolare l'effetto Symlin. Le caratteristiche demografiche e basali per gli 871 pazienti trattati con Symlin sono le seguenti: HbA1c basale medio variava da 9,0 a 9,4%, età media compresa tra 56,4 e 59,1 anni, durata media del diabete compresa tra 11,5 e 14,4 anni e BMI medio compreso tra 30,1 e 34,4 kg / m2. In entrambi questi studi, Symlin o placebo sono stati aggiunti alle terapie per il diabete esistenti dei partecipanti, che includevano insulina con o senza un agente sulfonilurea e / o metformina.
La tabella 2 riassume i risultati compositi in entrambi gli studi per i pazienti assegnati alla dose di 120 mcg dopo 6 mesi di trattamento.
Tabella 2: Variazione media (SE) di HbA1c, peso e insulina a 6 mesi negli studi in doppio cieco, controllati con placebo, in pazienti con diabete di tipo 2 che utilizza insulina
| Variabile | Placebo | Symlin (120 mcg) |
|---|---|---|
| Basale HbA1c (%) | 9.3 (0.08) | 9.1 (0.06) |
| Variazione di HbA1c a 6 mesi rispetto al basale (%) | −0.17 (0.07) | −0.57 (0.06)* |
| Variazione HbA1c sottratta dal placebo a 6 mesi (%) | N / A | −0.40 (0.09)* |
| Peso basale (kg) | 91.3 (1.2) | 92.5 (1.2) |
| Variazione di peso a 6 mesi rispetto al basale (kg) | +0.2 (0.2) | −1.5 (0.2)* |
| Variazione di peso sottratta dal placebo a 6 mesi (kg) | N / A | −1.7 (0.3)* |
| Variazione percentuale delle dosi di insulina a 6 mesi: rapida / a breve durata d'azione | +6.5 (2.7) | −3.0 (1.6)* |
| Variazione percentuale delle dosi di insulina a 6 mesi: azione prolungata | +5.2 (1.4) | −0.2 (1.3)* |
|
In una coorte di 145 pazienti che hanno completato due anni di trattamento con Symlin, l'HbA1c sottratto al basale e le riduzioni di peso sono state: rispettivamente "0,40% e" 0,36 kg.
Studio in aperto in ambito clinico
È stato condotto uno studio in aperto di Symlin alla dose raccomandata di 120 mcg in 166 pazienti con diabete di tipo 2 che utilizzava insulina che non erano in grado di raggiungere obiettivi glicemici usando solo l'insulina. In questi pazienti è stato impiegato un regime di insulina a dose flessibile (vedere DOSAGGIO E SOMMINISTRAZIONE). In questo studio, i pazienti hanno modificato il regime di insulina in base al monitoraggio del glucosio pre e post pasto. Al basale, l'HbA1c medio era dell'8,3%, l'età media era di 54,4 anni, la durata media del diabete era di 13,3 anni e l'IMC medio era di 38,6 kg / m2. Symlin è stato somministrato con pasti importanti. Il trattamento con Symlin più insulina per 6 mesi ha comportato una riduzione media dell'HbA1c sottratta al basale di "0,56 ± 0,15% e una riduzione del peso medio sottratta al basale di" 2,76 ± 0,34 kg. Questi cambiamenti sono stati realizzati con riduzioni delle dosi di insulina totale, a breve durata d'azione e a lunga durata d'azione ("6,4 ± 2,66," 10,3 ± 4,84 e "4,2 ± 2,42%, rispettivamente).
Studi clinici sul diabete di tipo 1
L'efficacia di una gamma di dosi di Symlin è stata valutata in numerosi studi clinici controllati verso placebo e in aperto condotti su pazienti con diabete di tipo 1. Sulla base dei risultati ottenuti in questi studi, la dose raccomandata di Symlin per i pazienti con diabete di tipo 1 è di 30 mcg o 60 mcg somministrati immediatamente prima dei pasti principali.
Sono stati condotti tre studi a lungo termine (da 26 a 52 settimane), randomizzati, in doppio cieco, controllati con placebo su Symlin in pazienti con diabete di tipo 1 (N = 1717). Due di questi studi hanno consentito solo un minimo aggiustamento dell'insulina al fine di isolare l'effetto Symlin; nel terzo studio, gli aggiustamenti dell'insulina sono stati effettuati secondo la pratica medica standard. Le caratteristiche demografiche e basali per i 1179 pazienti trattati con Symlin erano le seguenti: l'intervallo HbA1c basale medio era compreso tra 8,7 e 9,0%, intervallo di età medio compreso tra 37,3 e 41,9 anni, durata media dell'intervallo di diabete tra 15,5 e 19,2 anni e intervallo di BMI medio compreso tra 25,0 e 26,8 kg / m2. Symlin o placebo sono stati aggiunti alle terapie insuliniche esistenti.
La tabella 3 riassume i risultati compositi di questi studi per i pazienti assegnati alla dose di 30 o 60 mcg dopo 6 mesi di trattamento.
Tabella 3: Variazione media (SE) di HbA1c, peso e insulina a 6 mesi negli studi in doppio cieco, controllati con placebo, in pazienti con diabete di tipo 1
| Variabile | Placebo | Symlin (30 o 60 mcg) |
|---|---|---|
| Basale HbA1c (%) | 9.0 (0.06) | 8.9 (0.04) |
| Variazione di HbA1c a 6 mesi rispetto al basale (%) | −0.10 (0.05) | −0.43 (0.04)* |
| Variazione HbA1c sottratta dal placebo a 6 mesi (%) | N / A | −0.33 (0.06)* |
| Peso basale (kg) | 75.1 (0.6) | 76.1 (0.5) |
| Variazione di peso a 6 mesi rispetto al basale (kg) | +0.6 (0.1) | −1.1 (0.1)* |
| Variazione di peso sottratta dal placebo a 6 mesi (kg) | N / A | −1.7 (0.1)* |
| Variazione percentuale delle dosi di insulina a 6 mesi: rapida / a breve durata d'azione | +1.7 (3.3) | −3.6 (2.9) |
| Variazione percentuale delle dosi di insulina a 6 mesi: azione prolungata | +2.5 (1.9) | +1.9 (1.3) |
|
* Riduzione statisticamente significativa rispetto al placebo (valore p <0,05). |
In una coorte di 73 pazienti che hanno completato due anni di trattamento con Symlin, l'HbA1c sottratto al basale e le variazioni di peso sono state: rispettivamente 0,35% e 0,60 kg.
Versione di prova della titolazione della dose di Symlin
È stato condotto uno studio sulla titolazione della dose di Symlin in pazienti con diabete di tipo 1. I pazienti con controllo glicemico basale relativamente buono (media HbA1c = 8,1%) sono stati randomizzati a ricevere insulina più placebo o insulina più Symlin. Altre caratteristiche basali e demografiche erano: età media di 41 anni, durata media del diabete di 20 anni, indice di massa corporea medio di 28 kg / m2. Symlin è stato iniziato a una dose di 15 mcg e titolato verso l'alto a intervalli settimanali con incrementi di 15 mcg a dosi di 30 mcg o 60 mcg, in base al fatto che i pazienti abbiano manifestato nausea. Una volta raggiunta una dose tollerata di 30 mcg o 60 mcg, la dose di Symlin è stata mantenuta per il resto dello studio (Symlin è stato somministrato prima dei pasti principali). Durante la titolazione di Symlin, la dose di insulina (principalmente l'insulina ad azione breve / rapida) è stata ridotta del 30-50% al fine di ridurre l'insorgenza di ipoglicemia. Una volta raggiunta una dose tollerata di Symlin, sono stati effettuati aggiustamenti della dose di insulina secondo la pratica clinica standard, sulla base del monitoraggio della glicemia pre e post pasto. Entro 6 mesi di trattamento, i pazienti trattati con Symlin e insulina e i pazienti trattati con insulina e placebo hanno avuto riduzioni equivalenti di HbA1c medio (7 0,47 ± 0,07% vs. "0,49 ± 0,07%, rispettivamente); i pazienti in trattamento con Symlin hanno perso peso ("1,33 ± 0,31 kg rispetto al basale e" 2,6 kg rispetto al placebo più i pazienti trattati con insulina). I pazienti trattati con Symlin hanno usato meno insulina totale ("11,7% rispetto al basale) e meno insulina a breve / rapida azione (" 22,8%) rispetto al basale.
Studio in aperto in ambito clinico
Uno studio in aperto di Symlin è stato condotto in pazienti con diabete di tipo 1 che non erano in grado di raggiungere obiettivi glicemici usando solo insulina. In questi pazienti è stato impiegato un regime di insulina a dose flessibile dopo il completamento della titolazione di Symlin (vedere DOSAGGIO E SOMMINISTRAZIONE). In questo studio, i pazienti hanno modificato il regime di insulina in base al monitoraggio del glucosio pre e post pasto. Al basale, l'HbA1c medio era dell'8,0%, l'età media era di 42,7 anni, la durata media del diabete era di 21,2 anni e l'IMC medio era di 28,6 kg / m2. Il dosaggio giornaliero di Symlin era di 30 mcg o 60 mcg con i pasti principali.
Symlin più insulina hanno ridotto l'HbA1c e il peso corporeo rispetto al basale a 6 mesi in media rispettivamente dello 0,18% e 3,0 kg. Questi cambiamenti nel controllo glicemico e nel peso corporeo sono stati raggiunti con riduzioni delle dosi totali, insulina a breve e lunga durata ("12 ± ± 1,36," 21,7 ± 2,81 e "± ± 1,59%, rispettivamente).
superiore
Indicazioni e utilizzo
Symlin viene somministrato durante i pasti ed è indicato per:
- Diabete di tipo 1, come trattamento aggiuntivo nei pazienti che usano la terapia insulinica durante i pasti e che non sono riusciti a ottenere il controllo desiderato del glucosio nonostante la terapia insulinica ottimale.
- Diabete di tipo 2, come trattamento aggiuntivo nei pazienti che usano la terapia insulinica durante i pasti e che non sono riusciti a raggiungere controllo desiderato del glucosio nonostante terapia insulinica ottimale, con o senza un agente simultaneo della sulfonilurea e / o metformina.
superiore
Controindicazioni
Symlin è controindicato nei pazienti con uno dei seguenti:
- un'ipersensibilità nota a Symlin o ad uno qualsiasi dei suoi componenti, incluso metacresolo;
- una diagnosi confermata di gastroparesi;
- inconsapevolezza di ipoglicemia.
superiore
Avvertenze
Selezione del paziente
La corretta selezione dei pazienti è fondamentale per un uso sicuro ed efficace di Symlin
Prima di iniziare la terapia, è necessario rivedere l'HbA1c del paziente, i recenti dati di monitoraggio della glicemia, la storia di ipoglicemia indotta da insulina, l'attuale regime di insulina e il peso corporeo. La terapia con Symlin deve essere presa in considerazione solo in pazienti con diabete di tipo 2 o di tipo 1 insulino che soddisfano i seguenti criteri:
- non sono riusciti a raggiungere un adeguato controllo glicemico nonostante la gestione individualizzata dell'insulina;
- stanno ricevendo cure continue sotto la guida di un operatore sanitario specializzato nell'uso dell'insulina e supportato dai servizi di educatori del diabete.
I pazienti che soddisfano uno dei seguenti criteri NON devono essere considerati per la terapia con Symlin:
- scarsa conformità con l'attuale regime di insulina;
- scarsa conformità con il monitoraggio prescritto della glicemia;
- avere un HbA1c> 9%;
- ipoglicemia grave ricorrente che richiede assistenza negli ultimi 6 mesi;
- presenza di inconsapevolezza di ipoglicemia;
- diagnosi confermata di gastroparesi;
- richiedere l'uso di farmaci che stimolano la motilità gastrointestinale;
- pazienti pediatrici.
L'ipoglicemia
Symlin da solo non causa ipoglicemia. Tuttavia, Symlin è indicato per la co-somministrazione con terapia insulinica e in questa impostazione Symlin aumenta il rischio di ipoglicemia grave indotta da insulina, in particolare nei pazienti di tipo 1 diabete. L'ipoglicemia grave associata a Symlin si verifica entro le prime 3 ore dopo un'iniezione di Symlin. Se si verifica una grave ipoglicemia durante la guida di un veicolo a motore, macchinari pesanti o durante altre attività ad alto rischio, possono verificarsi lesioni gravi. Pertanto, quando si introduce la terapia con Symlin, è necessario prendere le opportune precauzioni per evitare di aumentare il rischio di ipoglicemia grave indotta dall'insulina. Queste precauzioni includono un frequente monitoraggio del glucosio pre e post pasto combinato con una riduzione iniziale del 50% delle dosi pre-pasto di insulina ad azione breve (vedere DOSAGGIO E SOMMINISTRAZIONE).
I sintomi dell'ipoglicemia possono includere fame, mal di testa, sudorazione, tremore, irritabilità o difficoltà di concentrazione. Le rapide riduzioni delle concentrazioni di glucosio nel sangue possono indurre tali sintomi indipendentemente dai valori di glucosio. I sintomi più gravi di ipoglicemia includono perdita di coscienza, coma o convulsioni.
I sintomi di allarme precoce dell'ipoglicemia possono essere diversi o meno pronunciati in determinate condizioni, come la lunga durata del diabete; malattia del nervo diabetico; uso di farmaci come beta-bloccanti, clonidina, guanetidina o reserpina; o intensificato controllo del diabete.
L'aggiunta di qualsiasi agente antiiperglicemico come Symlin a un regime esistente di uno o più agenti antiiperglicemici (ad es. Insulina, sulfonilurea), oppure altri agenti che possono aumentare il rischio di ipoglicemia possono richiedere ulteriori aggiustamenti della dose di insulina e un monitoraggio particolarmente attento della glicemia.
I seguenti sono esempi di sostanze che possono aumentare l'effetto ipoglicemizzante e la suscettibilità all'ipoglicemia: antidiabetico orale prodotti, ACE-inibitori, diisopiramide, fibrati, fluoxetina, inibitori MAO, pentossifillina, propossifene, salicilati e sulfonamide antibiotici.
Gli studi clinici che utilizzano una sfida ipoglicemizzante controllata hanno dimostrato che Symlin non altera la risposta ormonale controregolatoria all'ipoglicemia indotta dall'insulina. Allo stesso modo, nei pazienti trattati con Symlin, la percezione dei sintomi ipoglicemici non è stata modificata con concentrazioni plasmatiche di glucosio a partire da 45 mg / dL.
superiore
Precauzioni
Generale
Ipoglicemia (Vedi AVVERTENZE).
Symlin deve essere prescritto con cautela alle persone con disabilità visiva o di destrezza.
Informazioni per i pazienti
Gli operatori sanitari dovrebbero informare i pazienti dei potenziali rischi e vantaggi della terapia con Symlin. Gli operatori sanitari dovrebbero anche informare i pazienti sulle pratiche di autogestione, incluso il monitoraggio del glucosio, la corretta tecnica di iniezione, i tempi di somministrazione e la corretta conservazione di Symlin. Inoltre, rafforzare l'importanza dell'adesione alla pianificazione dei pasti, all'attività fisica, al riconoscimento e alla gestione dell'ipoglicemia e dell'iperglicemia e alla valutazione delle complicanze del diabete. Per ulteriori informazioni, consultare la Guida ai farmaci Symlin e le Istruzioni per l'uso del paziente.
Istruire i pazienti sulla gestione di situazioni speciali come condizioni intercorrenti (malattia o stress), inadeguata o omessa dose di insulina, somministrazione involontaria di aumento della dose di insulina o Symlin, assunzione di cibo inadeguata o mancato pasti.
Symlin e insulina devono essere sempre somministrati come iniezioni separate e non devono mai essere miscelati.
Le donne con diabete dovrebbero essere informate di informare il proprio medico in caso di gravidanza o in gravidanza.
Insufficienza renale
I requisiti di dosaggio per Symlin non sono alterati nei pazienti con insufficienza renale moderata o grave (ClCr> 20 a â ‰ ¤50 ml / min). Non sono stati condotti studi su pazienti in dialisi (vedere FARMACOLOGIA CLINICA; Popolazioni speciali).
Insufficienza epatica
Non sono stati condotti studi su pazienti con insufficienza epatica. Tuttavia, non si prevede che la disfunzione epatica influenzi le concentrazioni ematiche di Symlin (vedere FARMACOLOGIA CLINICA; Popolazioni speciali).
Allergia
Allergia locale
I pazienti possono manifestare arrossamento, gonfiore o prurito nel sito di iniezione. Queste reazioni minori di solito si risolvono in pochi giorni o alcune settimane. In alcuni casi, queste reazioni possono essere correlate a fattori diversi da Symlin, come irritanti in un detergente per la pelle o tecnica di iniezione impropria.
Allergia sistemica
In studi clinici controllati fino a 12 mesi, sono state segnalate potenziali reazioni allergiche sistemiche in 65 (5%) pazienti di tipo 2 e 59 (5%) pazienti trattati con Symlin di tipo 1. Reazioni simili sono state riportate da 18 (4%) e 28 (5%) pazienti di tipo 2 e di tipo 1 trattati con placebo, rispettivamente. Nessun paziente in trattamento con Symlin è stato ritirato da una sperimentazione a causa di una potenziale reazione allergica sistemica.
Interazioni farmacologiche
A causa dei suoi effetti sullo svuotamento gastrico, la terapia con Symlin non deve essere presa in considerazione per i pazienti che assumono farmaci che alterano il tratto gastrointestinale motilità (ad es. agenti anticolinergici come l'atropina) e agenti che rallentano l'assorbimento intestinale dei nutrienti (ad es. α-glucosidasi inibitori). I pazienti che usano questi farmaci non sono stati studiati negli studi clinici.
Symlin ha il potenziale per ritardare l'assorbimento di farmaci orali somministrati in concomitanza. Quando la rapida insorgenza di un agente concomitante somministrato per via orale è un fattore determinante critico per l'efficacia (come analgesici), l'agente deve essere somministrato almeno 1 ora prima o 2 ore dopo Symlin iniezione.
Negli studi clinici, l'uso concomitante di sulfoniluree o biguanidi non ha modificato il profilo degli eventi avversi di Symlin. Non sono stati condotti studi formali di interazione per valutare l'effetto di Symlin sulla cinetica degli agenti antidiabetici orali.
Mescolando Symlin e Insulina
I parametri farmacocinetici di Symlin sono stati alterati quando miscelati con formulazioni premiscelate regolari, NPH e 70/30 di insulina umana ricombinante immediatamente prima dell'iniezione. Pertanto, Symlin e insulina non devono essere miscelati e devono essere somministrati separatamente.
Cancerogenesi, mutagenesi, alterazione della fertilità
cancerogenesi
Uno studio di carcinogenicità di due anni è stato condotto su topi CD-1 con dosi di 0,2, 0,5 e 1,2 mg / kg / giorno di Symlin (32, 67 e 159 volte l'esposizione risultante dalla dose umana massima raccomandata basata sull'area al di sotto della curva di concentrazione plasmatica o dell'AUC, rispettivamente). Non sono stati osservati tumori indotti da farmaci. Uno studio di carcinogenicità di due anni è stato condotto su ratti Sprague-Dawley con dosi di 0,04, 0,2 e 0,5 mg / kg / giorno di Symlin (3, 9 e 25 volte l'esposizione risultante dalla dose massima raccomandata nell'uomo in base all'AUC, rispettivamente). Non sono stati osservati tumori indotti da farmaci in nessun organo.
mutagenesi
Symlin non è risultato mutageno nel test di Ames e non ha aumentato l'aberrazione cromosomica nel test sui linfociti umani. Symlin non era clastogenico nel test del micronucleo su topo in vivo o nel test di aberrazione cromosomica utilizzando cellule ovariche di criceto cinese.
Compromissione della fertilità
Somministrazione di 0,3, 1 o 3 mg / kg / giorno di Symlin (8, 17 e 82 volte l'esposizione risultante dal massimo dose umana raccomandata basata sulla superficie corporea) non ha avuto effetti significativi sulla fertilità negli uomini o nelle donne ratti. La dose più elevata di 3 mg / kg / die ha provocato distocia in 8/12 femmine di ratto secondarie a significative riduzioni dei livelli sierici di calcio.
Gravidanza
Effetti teratogeni: gravidanza categoria C
Non sono stati condotti studi adeguati e ben controllati su donne in gravidanza. Gli studi sulla placenta umana perfusa indicano che Symlin ha un basso potenziale di attraversamento della barriera placentare materna / fetale. Studi di tossicità embriofetale con Symlin sono stati condotti su ratti e conigli. Sono stati osservati aumenti delle anomalie congenite (difetto del tubo neurale, palatoschisi, esencefalia) nei feti di ratti trattati durante organogenesi con 0,3 e 1,0 mg / kg / die (10 e 47 volte l'esposizione risultante dalla dose massima raccomandata nell'uomo in base all'AUC, rispettivamente). La somministrazione di dosi fino a 0,3 mg / kg / die Symlin (9 volte la dose massima raccomandata in base all'AUC) ai conigli in gravidanza non ha avuto effetti negativi sullo sviluppo embrio-fetale; tuttavia, gli studi sulla riproduzione animale non sono sempre predittivi della risposta umana. Symlin deve essere usato durante la gravidanza solo se è stabilito dal personale sanitario che il potenziale beneficio giustifica il potenziale rischio per il feto.
Madri che allattano
Non è noto se Symlin sia escreto nel latte materno. Molti farmaci, compresi i peptidi, vengono escreti nel latte materno. Pertanto, Symlin deve essere somministrato alle donne che allattano solo se è stabilito dal personale sanitario che il potenziale beneficio supera il potenziale rischio per il bambino.
Uso pediatrico
La sicurezza e l'efficacia di Symlin nei pazienti pediatrici non sono state stabilite.
Uso geriatrico
Symlin è stato studiato in pazienti di età compresa tra 15 e 84 anni, inclusi 539 pazienti di età pari o superiore a 65 anni. La variazione dei valori di HbA1c e delle frequenze di ipoglicemia non differiva in base all'età, ma non si può escludere una maggiore sensibilità in alcuni soggetti più anziani. Pertanto, sia i regimi Symlin che quelli insulinici devono essere attentamente gestiti per ovviare ad un aumentato rischio di grave ipoglicemia.
superiore
Reazioni avverse
Eventi avversi (esclusa l'ipoglicemia, discussi di seguito) comunemente associati a Symlin quando co-somministrato con una dose fissa di insulina in gli studi a lungo termine controllati con placebo su pazienti di tipo 2 e di tipo 1 che utilizzano insulina sono presentati nella Tabella 4 e nella Tabella 5, rispettivamente. Gli stessi eventi avversi sono stati evidenziati anche nello studio di pratica clinica in aperto, che ha impiegato il dosaggio flessibile dell'insulina.
Tabella 4: Eventi avversi emergenti dal trattamento che si verificano con un'incidenza del 5% e una maggiore incidenza con Symlin rispetto al placebo in studi a lungo termine controllati con placebo. Incidenza degli stessi eventi nello studio di pratica clinica in aperto (pazienti con diabete di tipo 2 che utilizza insulina, 120 mcg)
| Studi a lungo termine controllati con placebo | Studio di pratica clinica in aperto | ||
|---|---|---|---|
| Placebo + Insulina (N (%)) (N = 284) |
Symlin + Insulina (N (%)) (N = 292) |
Symlin + Insulina (N (%)) (N = 166) |
|
| Nausea | 34 (12) | 81 (28) | 53 (30) |
| Mal di testa | 19 (7) | 39 (13) | 8 (5) |
| Anoressia | 5 (2) | 27 (9) | 1 (<1) |
| vomito | 12 (4) | 24 (8) | 13 (7) |
| Dolore addominale | 19 (7) | 23 (8) | 3 (2) |
| Fatica | 11 (4) | 20 (7) | 5 (3) |
| Vertigini | 11 (4) | 17 (6) | 3 (2) |
| tosse | 12 (4) | 18 (6) | 4 (2) |
| Faringite | 7 (2) | 15 (5) | 6 (3) |
Tabella 5: Eventi avversi emergenti dal trattamento che si verificano con un'incidenza del 5% e una maggiore incidenza con Symlin rispetto al placebo in studi a lungo termine controllati con placebo. Incidenza degli stessi eventi nello studio di pratica clinica in aperto (pazienti con diabete di tipo 1, 30 o 60 mcg)
| Studi a lungo termine controllati con placebo | Studio di pratica clinica in aperto | ||
|---|---|---|---|
| Placebo + insulina (n (%)) (N = 538) |
Symlin + Insulina (n (%)) (N = 716) |
Symlin + Insulina (n (%)) (N = 265) |
|
| Nausea | 92 (17) | 342 (48) | 98 (37) |
| Anoressia | 12 (2) | 122 (17) | 0 (0) |
| Lesione inflitta | 55 (10) | 97 (14) | 20 (8) |
| vomito | 36 (7) | 82 (11) | 18 (7) |
| artralgia | 27 (5) | 51 (7) | 6 (2) |
| Fatica | 22 (4) | 51 (7) | 12 (4.5) |
| Reazione allergica | 28 (5) | 41 (6) | 1 (<1) |
| Vertigini | 21 (4) | 34 (5) | 5 (2) |
La maggior parte degli eventi avversi erano di natura gastrointestinale. Nei pazienti con diabete di tipo 2 o di tipo 1, l'incidenza di nausea era più alta all'inizio del trattamento con Symlin e diminuiva con il tempo nella maggior parte dei pazienti. L'incidenza e la gravità della nausea si riducono quando Symlin viene gradualmente titolato alle dosi raccomandate (vedere DOSAGGIO E SOMMINISTRAZIONE).
Ipoglicemia grave
Symlin da solo (senza la concomitante somministrazione di insulina) non provoca ipoglicemia. Tuttavia, Symlin è indicato come trattamento aggiuntivo nei pazienti che usano la terapia insulinica durante i pasti e la co-somministrazione di Symlin con insulina può aumentare il rischio di ipoglicemia indotta da insulina, in particolare nei pazienti con diabete di tipo 1 (vedere Avviso in scatola). L'incidenza di ipoglicemia grave durante il programma di sviluppo clinico Symlin è riassunta nella Tabella 6 e nella Tabella 7.
Tabella 6: Incidenza e tasso di eventi di ipoglicemia grave negli studi clinici a lungo termine, controllati con placebo e in aperto, in studi clinici su pazienti con diabete di tipo 2 che utilizza insulina
| Lungo termine, Studi controllati con placebo (Nessuna riduzione della dose di insulina durante l'inizio) |
Etichetta aperta, Studio di pratica clinica (Riduzione della dose di insulina durante l'inizio) |
|||||
|---|---|---|---|---|---|---|
| Placebo + Insulina | Symlin + Insulina | Symlin + Insulina | ||||
|
Ipoglicemia grave |
0-3 mesi (N = 284) |
>3-6 mesi (N = 251) |
0-3 mesi (N = 292) |
>3-6 mesi (N = 255) |
0-3 mesi (N = 166) |
>3-6 mesi (N = 150) |
| Paziente-accertate * | ||||||
| Frequenza eventi (frequenza eventi / anno paziente) | 0.24 | 0.13 | 0.45 | 0.39 | 0.05 | 0.03 |
| Incidenza (%) | 2.1 | 2.4 | 8.2 | 4.7 | 0.6 | 0.7 |
| Assistenza medicaâ € | ||||||
| Frequenza eventi (frequenza eventi / anno paziente) | 0.06 | 0.07 | 0.09 | 0.02 | 0.05 | 0.03 |
| Incidenza (%) | 0.7 | 1.2 | 1.7 | 0.4 | 0.6 | 0.7 |
|
* Ipoglicemia grave accertata dal paziente: richiesta l'assistenza di un altro individuo (incluso l'aiuto nell'ingestione di carboidrati orali); e / o richiedere la somministrazione di iniezione di glucagone, glucosio endovenoso o altri interventi medici. • Ipoglicemia grave assistita dal punto di vista medico: richiesta di glucagone, glucosio EV, ricovero ospedaliero, assistenza paramedica, visita al pronto soccorso e / o valutazione come SAE da parte dello sperimentatore. |
Tabella 7: Incidenza e tasso di eventi di ipoglicemia grave negli studi clinici a lungo termine, controllati con placebo e in aperto, in studi clinici su pazienti con diabete di tipo 1
| Lungo termine, Studi controllati con placebo (Nessuna riduzione della dose di insulina durante l'inizio) |
Etichetta aperta, Studio di pratica clinica (Riduzione della dose di insulina durante l'inizio) |
|||||
|---|---|---|---|---|---|---|
| Placebo + Insulina | Symlin + Insulina | Symlin + Insulina | ||||
|
Ipoglicemia grave |
0-3 mesi (N = 538) |
>3-6 mesi (N = 470) |
0-3 mesi (N = 716) |
>3-6 mesi (N = 576) |
0-3 mesi (N = 265) |
>3-6 mesi (N = 213) |
| Paziente-accertate * | ||||||
| Frequenza eventi (frequenza eventi / anno paziente) | 1.33 | 1.06 | 1.55 | 0.82 | 0.29 | 0.16 |
| Incidenza (%) | 10.8 | 8.7 | 16.8 | 11.1 | 5.7 | 3.8 |
| Assistenza medicaâ € | ||||||
| Frequenza eventi (frequenza eventi / anno paziente) | 0.19 | 0.24 | 0.50 | 0.27 | 0.10 | 0.04 |
| Incidenza (%) | 3.3 | 4.3 | 7.3 | 5.2 | 2.3 | 0.9 |
|
* Ipoglicemia grave accertata dal paziente: richiesta l'assistenza di un altro individuo (incluso l'aiuto nell'ingestione di carboidrati orali); e / o richiedere la somministrazione di iniezione di glucagone, glucosio endovenoso o altri interventi medici. • Ipoglicemia grave assistita dal punto di vista medico: richiesta di glucagone, glucosio EV, ricovero ospedaliero, assistenza paramedica, visita al pronto soccorso e / o valutazione come SAE da parte dello sperimentatore. |
Esperienza post marketing
Dall'introduzione sul mercato di Symlin, sono state riportate le seguenti reazioni avverse. Poiché questi eventi sono segnalati volontariamente da una popolazione di dimensioni incerte, non è sempre possibile stimare in modo affidabile la loro frequenza o stabilire una relazione causale con l'esposizione al farmaco.
Generale: reazioni nel sito di iniezione.
Overdose
Dosi singole da 10 mg di Symlin (83 volte la dose massima di 120 mcg) sono state somministrate a tre volontari sani. In tutti e tre i soggetti è stata osservata grave nausea associata a vomito, diarrea, vasodilatazione e vertigini. Non è stata segnalata ipoglicemia. Symlin ha una breve emivita e in caso di sovradosaggio sono indicate misure di supporto.
superiore
Dosaggio e amministrazione
Il dosaggio di Symlin varia a seconda che il paziente abbia il diabete di tipo 2 o di tipo 1 (vedere sotto). Quando si inizia la terapia con Symlin, è richiesta una riduzione iniziale della dose di insulina in tutti i pazienti (sia di tipo 2 che di tipo 1) per ridurre il rischio di ipoglicemia indotta dall'insulina. Poiché questa riduzione dell'insulina può portare ad aumenti del glucosio, i pazienti devono essere monitorati ad intervalli regolari per valutare la tollerabilità di Symlin e l'effetto sulla glicemia, in modo che possano essere aggiustamenti individuali dell'insulina iniziati. Se la terapia con Symlin viene interrotta per qualsiasi motivo (ad es., Chirurgia o malattie), lo stesso protocollo di avvio deve essere seguito quando viene ripristinata la terapia con Symlin (vedere di seguito).
Inizio della terapia con Symlin
Pazienti con diabete di tipo 2 a insulina
Nei pazienti con diabete di tipo 2 che utilizza insulina, Symlin deve essere iniziato a una dose di 60 mcg e aumentato a una dose di 120 mcg come tollerato.
I pazienti devono essere istruiti a:
- Avviare Symlin a 60 mcg per via sottocutanea, immediatamente prima dei pasti principali;
- Ridurre del 50% i dosaggi di insulina preprandiale, ad azione rapida o ad azione breve, comprese le insuline a miscelazione fissa (70/30);
- Monitorare frequentemente la glicemia, inclusi i pasti prima e dopo i pasti e prima di coricarsi;
- Aumentare la dose di Symlin a 120 mcg quando non si è verificata nausea clinicamente significativa per 3-7 giorni. Gli aggiustamenti della dose di Symlin devono essere effettuati solo come indicato dall'operatore sanitario. Se persiste una significativa nausea alla dose di 120 mcg, la dose di Symlin deve essere ridotta a 60 mcg;
- Regolare le dosi di insulina per ottimizzare il controllo glicemico una volta raggiunta la dose target di Symlin e la nausea (se sperimentata) è diminuita. Gli aggiustamenti della dose di insulina devono essere effettuati solo come indicato dall'operatore sanitario;
- Contattare un operatore sanitario esperto nell'uso dell'insulina per rivedere almeno gli aggiustamenti della dose di Symlin e insulina una volta alla settimana fino al raggiungimento di una dose target di Symlin, Symlin è ben tollerato e le concentrazioni di glucosio nel sangue lo sono stabile.
Pazienti con diabete di tipo 1
Nei pazienti con diabete di tipo 1, Symlin deve essere iniziato a una dose di 15 mcg e titolato a incrementi di 15 mcg a una dose di mantenimento di 30 mcg o 60 mcg come tollerato.
I pazienti devono essere istruiti a:
- Avviare Symlin alla dose iniziale di 15 mcg per via sottocutanea, immediatamente prima dei pasti principali;
- Ridurre del 50% i dosaggi di insulina preprandiale, ad azione rapida o ad azione breve, comprese le insuline a miscelazione fissa (ad es. 70/30);
- Monitorare frequentemente la glicemia, inclusi i pasti prima e dopo i pasti e prima di coricarsi;
- Aumentare la dose di Symlin all'incremento successivo (30 mcg, 45 mcg o 60 mcg) quando non si è verificata nausea clinicamente significativa per almeno 3 giorni. Gli aggiustamenti della dose di Symlin devono essere effettuati solo come indicato dall'operatore sanitario. Se la nausea significativa persiste alla dose di 45 o 60 mcg, la dose di Symlin deve essere ridotta a 30 mcg. Se la dose di 30 mcg non è tollerata, deve essere presa in considerazione l'interruzione della terapia con Symlin;
- Regolare le dosi di insulina per ottimizzare il controllo glicemico una volta raggiunta la dose target di Symlin e la nausea (se sperimentata) è diminuita. Gli aggiustamenti della dose di insulina devono essere effettuati solo come indicato dall'operatore sanitario;
- Contattare un operatore sanitario esperto nell'uso dell'insulina per rivedere almeno gli aggiustamenti della dose di Symlin e insulina una volta alla settimana fino al raggiungimento di una dose target di Symlin, Symlin è ben tollerato e le concentrazioni di glucosio nel sangue lo sono stabile.
Una volta raggiunta la dose target di Symlin nei pazienti di tipo 2 o di tipo 1
Dopo aver raggiunto una dose di mantenimento di Symlin, sia i pazienti che usano insulina con diabete di tipo 2 che i pazienti con diabete di tipo 1 devono essere istruiti a:
- Regolare le dosi di insulina per ottimizzare il controllo glicemico una volta raggiunta la dose target di Symlin e la nausea (se sperimentata) è diminuita. Gli aggiustamenti della dose di insulina devono essere effettuati solo come indicato da un operatore sanitario;
- Contattare un operatore sanitario in caso di nausea o ipoglicemia ricorrenti. Un'aumentata frequenza di ipoglicemia da lieve a moderata deve essere vista come un segnale di avvertimento di un aumentato rischio di ipoglicemia grave.
Amministrazione
Symlin deve essere somministrato per via sottocutanea immediatamente prima di ogni pasto principale (â ‰ ¥ 250 kcal o contenente ‰ ¥ 30 g di carboidrati).
Symlin deve essere a temperatura ambiente prima dell'iniezione per ridurre le potenziali reazioni nel sito di iniezione. Ogni dose di Symlin deve essere somministrata per via sottocutanea nell'addome o nella coscia (la somministrazione nel braccio non è raccomandata a causa dell'assorbimento variabile). I siti di iniezione devono essere ruotati in modo tale che lo stesso sito non venga utilizzato ripetutamente. Il sito di iniezione selezionato deve anche essere distinto dal sito scelto per qualsiasi iniezione di insulina concomitante.
- Symlin e insulina devono essere sempre somministrati come iniezioni separate.
- Symlin non deve essere miscelato con nessun tipo di insulina.
- Se si dimentica una dose di Symlin, attendere fino alla successiva dose programmata e somministrare la normale dose.
Iniettore di penna SymlinPen®
L'iniettore di penna SymlinPen® è disponibile in due presentazioni:
- Iniettore di penna SymlinPen® 60 per dosi di 15 mcg, 30 mcg, 45 mcg, 60 mcg.
- Iniettore di penna SymlinPen® 120 per dosi da 60 mcg e 120 mcg.
Vedere le istruzioni per l'uso del paziente per le istruzioni per l'uso dell'iniettore penna SymlinPen®.
Il paziente deve essere avvisato:
- per confermare che stanno usando l'iniettore di penna corretto che erogherà la dose prescritta;
- sull'uso corretto dell'iniettore penna, sottolineando come e quando istituire un nuovo iniettore penna;
- non trasferire Symlin dall'iniettore della penna a una siringa. Ciò potrebbe comportare una dose più elevata del previsto, poiché Symlin nell'iniettore di penna ha una concentrazione più elevata di Symlin nella fiala di Symlin;
- di non condividere l'iniettore e gli aghi con gli altri;
- che gli aghi non sono inclusi con l'iniettore della penna e devono essere acquistati separatamente;
- quale lunghezza dell'ago e calibro dovrebbe essere usato;
- usare un nuovo ago per ogni iniezione.
Fiale Symlin
Per somministrare Symlin dai flaconcini, utilizzare una siringa da insulina U-100 (preferibilmente una dimensione di 0,3 mL [0,3 cc]) per una precisione ottimale. Se si utilizza una siringa calibrata per l'uso con insulina U-100, utilizzare la tabella seguente (Tabella 8) per misurare il dosaggio di microgrammi in incrementi di unità.
Tabella 8: conversione della dose di Symlin in equivalenti di unità di insulina
| Dosaggio prescritto (mcg) | Incremento usando una siringa U-100 (unità) | Volume (cc o mL) |
|---|---|---|
| 15 | 2 ½ | 0.025 |
| 30 | 5 | 0.05 |
| 45 | 7 ½ | 0.075 |
| 60 | 10 | 0.1 |
| 120 | 20 | 0.2 |
Usi sempre nuove siringhe e aghi nuovi per somministrare Symlin e iniezioni di insulina.
Interruzione della terapia
La terapia con Symlin deve essere interrotta se si verifica una delle seguenti condizioni:
* Ipoglicemia ricorrente inspiegabile che richiede assistenza medica;
* Nausea persistente clinicamente significativa;
* Non conformità con autocontrollo delle concentrazioni di glucosio nel sangue;
* Non conformità con aggiustamenti della dose di insulina;
* Non conformità con i contatti degli operatori sanitari programmati o le visite cliniche consigliate.
Preparazione e gestione
Symlin deve essere ispezionato visivamente per verificare la presenza di particelle o scolorimento prima della somministrazione ogni volta che la soluzione e il contenitore lo consentono.
superiore
Come fornito
Symlin viene fornito sotto forma di iniezione sterile nelle seguenti forme di dosaggio:
- 1,5 mL iniettore di penna monouso SymlinPen® 60 multidose contenente 1000 mcg / mL di pramlintide (come acetato).
- 2,7 mL iniettore di penna monouso SymlinPen® 120 multidose contenente 1000 mcg / mL di pramlintide (come acetato).
- Flaconcino da 5 mL, contenente 600 mcg / mL di pramlintide (come acetato), da utilizzare con una siringa da insulina.
Per somministrare Symlin dai flaconcini, utilizzare una siringa da insulina U-100 (preferibilmente una dimensione di 0,3 ml [0,3 cc]). Se si utilizza una siringa calibrata per l'uso con insulina U-100, utilizzare la tabella (Tabella 8) in DOSAGGIO E SOMMINISTRAZIONE sezione per misurare il dosaggio di microgrammi in incrementi di unità.
Non mescolare Symlin con insulina.
Symlin Injection è disponibile nelle seguenti confezioni:
- Iniettore di penna SymlinPen® 60, contenente 1000 mcg / mL di pramlintide (come acetato)
Iniettore di penna multidose monouso da 1,5 x 1,5 ml
(NDC 66780-115-02) - Iniettore di penna SymlinPen® 120, contenente 1000 mcg / mL di pramlintide (come acetato)
Iniettore di penna multidose usa e getta 2 X 2,7 mL
(NDC 66780-121-02) - Flaconcino da 5 mL, contenente 600 mcg / mL di pramlintide (come acetato), per l'uso con una siringa da insulina
(NDC 66780-110-01)
Conservazione
Iniettori e flaconcini Symlin non in uso: refrigerare (da 36 ° F a 46 ° F; Da 2 ° C a 8 ° C) e proteggere dalla luce. Non congelare. Non utilizzare se il prodotto è stato congelato. Symlin non utilizzato (aperto o non aperto) non deve essere utilizzato dopo la data di scadenza (SCAD) stampata sulla confezione e sull'etichetta.
Iniettori a penna e flaconcini Symlin in uso: dopo il primo utilizzo, conservare in frigorifero o conservare a una temperatura non superiore a 30 ° C (86 ° F) per 30 giorni. Utilizzare entro 30 giorni, anche refrigerato.
Le condizioni di conservazione sono riassunte nella Tabella 9.
Tabella 9: Condizioni di conservazione
| Forma di dosaggio | Non aperto (non in uso) refrigerato |
Apri (in uso) Refrigerato o Temperatura Fino a 86 ° F (30 ° C) |
|---|---|---|
| 1,5 mL di penna-iniettore 2,7 mL di penna-iniettore Flaconcino da 5 ml |
Fino alla data di scadenza | Utilizzare entro 30 giorni |
Gli iniettori e i flaconcini SymlinPen® SymlinPen® sono prodotti per: Amylin Pharmaceuticals, Inc. San Diego, CA 92121 USA 1-800-349-8919 http://www.Symlin.com
Solo Rx
Il marchio Symlin, il marchio di design Symlin e SymlinPen sono marchi registrati di Amylin Pharmaceuticals, Inc. Copyright © 2005-2008, Amylin Pharmaceuticals, Inc. Tutti i diritti riservati.
Ultimo aggiornamento: luglio 2008
Symlin, Symlin Pen, pramlintide acetato, informazioni per il paziente (in un inglese semplice)
Le informazioni contenute in questa monografia non intendono coprire tutti i possibili usi, indicazioni, precauzioni, interazioni farmacologiche o effetti avversi. Questa informazione è generalizzata e non è intesa come consulenza medica specifica. Se ha domande sui medicinali che sta assumendo o desidera ulteriori informazioni, consultare il medico, il farmacista o l'infermiere.
torna a: Sfoglia tutti i farmaci per il diabete



