Humalog per il trattamento del diabete
Marchi: Humalog Cartridge, Humalog KwikPen, Humalog Pen
Nome generico: insulina Lispro
Forma di dosaggio: iniezione
Descrizione
Farmacologia
Indicazioni e utilizzo
Controindicazioni
Avvertenze
Precauzioni
Interazioni farmacologiche
Reazioni avverse
Overdose
Dosaggio
Fornito
Humalog Pen, Humalog Cartridge, KwikPen, informazioni sul paziente insulina lispro (in inglese semplice)
Descrizione
Humalog® Mix75 / 25 ™ [75% di sospensione di insulina lispro protamina e 25% di iniezione di insulina lispro, (origine rDNA)] è una miscela di insulina lispro soluzione, un agente ipoglicemizzante ad azione rapida e sospensione di insulina lispro protamina, un ipoglicemizzante ad azione intermedia agente. Chimicamente, l'insulina lispro è analogo dell'insulina umana Lys (B28), Pro (B29), creato quando gli aminoacidi nelle posizioni 28 e 29 sulla catena B dell'insulina sono invertiti. L'insulina lispro è sintetizzata in uno speciale ceppo di laboratorio non patogeno di batteri Escherichia coli che è stato geneticamente modificato per produrre insulina lispro. La sospensione di insulina lispro protamina (componente NPL) è una sospensione di cristalli prodotta dalla combinazione di insulina lispro e protamina solfato in condizioni appropriate per la formazione di cristalli.
L'insulina lispro ha la seguente struttura primaria:

L'insulina lispro ha la formula empirica C257H383N65O77S6 e un peso molecolare di 5808, entrambi identici a quelli dell'insulina umana.
Le fiale e le penne Humalog Mix75 / 25 contengono una sospensione sterile di sospensione di insulina lispro protamina miscelata con insulina lispro solubile per l'uso come iniezione.
Ogni millilitro di iniezione Humalog Mix75 / 25 contiene insulina lispro 100 unità, 0,28 mg di protamina solfato, 16 mg di glicerina, 3,78 mg sodio fosfato dibasico, 1,76 mg di metacresolo, contenuto di ossido di zinco adeguato per fornire 0,025 mg di ione zinco, 0,715 mg di fenolo e acqua per Iniezione. Humalog Mix75 / 25 ha un pH compreso tra 7,0 e 7,8. Acido cloridrico al 10% e / o idrossido di sodio al 10% possono essere stati aggiunti per regolare il pH.
superiore
Farmacologia clinica
Attività antidiabetica
L'attività primaria dell'insulina, incluso Humalog Mix75 / 25, è la regolazione del metabolismo del glucosio. Inoltre, tutte le insuline hanno diverse azioni anaboliche e anti-cataboliche su molti tessuti del corpo. Nei muscoli e in altri tessuti (eccetto il cervello), l'insulina provoca un trasporto rapido di glucosio e aminoacidi a livello intracellulare, favorisce l'anabolismo e inibisce il catabolismo proteico. Nel fegato, l'insulina favorisce l'assorbimento e la conservazione del glucosio sotto forma di glicogeno, inibisce la gluconeogenesi e promuove la conversione del glucosio in eccesso in grasso.
L'insulina lispro, il componente ad azione rapida di Humalog Mix75 / 25, ha dimostrato di essere equipotente all'insulina umana regolare su base molare. Un'unità di Humalog® ha lo stesso effetto ipoglicemizzante di un'unità di insulina umana regolare, ma il suo effetto è più rapido e di durata più breve. Humalog Mix75 / 25 ha un analogo effetto ipoglicemizzante rispetto a Humulin® 70/30 su un'unità per unità di base.
farmacocinetica
Assorbimento
Gli studi condotti su soggetti non diabetici e pazienti con diabete di tipo 1 (insulino-dipendente) lo hanno dimostrato Humalog, il componente ad azione rapida di Humalog Mix75 / 25, viene assorbito più rapidamente dell'insulina umana regolare (U-100). Nei soggetti non diabetici trattati con dosi sottocutanee di Humalog comprese tra 0,1 e 0,4 U / kg, sono state osservate concentrazioni sieriche di picco da 30 a 90 minuti dopo la somministrazione. Quando i soggetti non diabetici hanno ricevuto dosi equivalenti di insulina umana regolare, le concentrazioni di picco di insulina si sono verificate tra 50 e 120 minuti dopo la somministrazione. Risultati simili sono stati osservati in pazienti con diabete di tipo 1.

Figura 1: Concentrazioni sieriche di insulina immunoreattiva (IRI), dopo iniezione sottocutanea di Humalog Mix75 / 25 o Humulin 70/30 in soggetti non diabetici sani.
Humalog Mix75 / 25 ha due fasi di assorbimento. La fase iniziale rappresenta l'insulina lispro e le sue distinte caratteristiche di rapida insorgenza. La fase tardiva rappresenta l'azione prolungata della sospensione di insulina lispro protamina. In 30 soggetti non diabetici sani trattati con dosi sottocutanee (0,3 U / kg) di Humalog Mix75 / 25, sono state osservate concentrazioni sieriche di picco da 30 a 240 minuti (mediana, 60 minuti) dopo la somministrazione (vedere Figura 1). Risultati identici sono stati trovati in pazienti con diabete di tipo 1. Le caratteristiche di assorbimento rapido di Humalog sono mantenute con Humalog Mix75 / 25 (vedi Figura 1).
La Figura 1 rappresenta la concentrazione sierica di insulina rispetto alle curve temporali di Humalog Mix75 / 25 e Humulin 70/30. Humalog Mix75 / 25 ha un assorbimento più rapido di Humulin 70/30, che è stato confermato in pazienti con diabete di tipo 1.
Distribuzione
Non sono stati condotti studi sulla distribuzione radiomarcata di Humalog Mix75 / 25. Tuttavia, il volume di distribuzione dopo l'iniezione di Humalog è identico a quello dell'insulina umana regolare, con un intervallo da 0,26 a 0,36 L / kg.
Metabolismo
Non sono stati condotti studi sul metabolismo umano di Humalog Mix75 / 25. Gli studi sugli animali indicano che il metabolismo di Humalog, il componente ad azione rapida di Humalog Mix75 / 25, è identico a quello dell'insulina umana regolare.
Eliminazione
Humalog Mix75 / 25 ha due fasi di assorbimento, una fase rapida e una fase prolungata, rappresentative dei componenti della sospensione dell'insulina lispro e dell'insulina lispro protamina. Come con altre insuline ad azione intermedia, non è possibile calcolare un'emivita significativa della fase terminale dopo somministrazione di Humalog Mix75 / 25 a causa della sospensione prolungata dell'insulina lispro protamina assorbimento.
farmacodinamica
Studi condotti su soggetti non diabetici e pazienti con diabete hanno dimostrato che Humalog ha un esordio più rapido attività ipoglicemizzante, un picco precedente per l'abbassamento del glucosio e una durata più breve dell'attività ipoglicemizzante rispetto Insulina umana regolare. L'inizio precoce dell'attività di Humalog Mix75 / 25 è direttamente correlato al rapido assorbimento di Humalog. Il corso dell'azione dell'insulina e degli analoghi dell'insulina, come Humalog (e quindi Humalog Mix75 / 25), può variare considerevolmente in soggetti diversi o all'interno dello stesso individuo. I parametri dell'attività Humalog Mix75 / 25 (tempo di insorgenza, ora di punta e durata) presentati nelle figure 2 e 3 devono essere considerati solo come linee guida generali. Il tasso di assorbimento di insulina e di conseguenza l'inizio dell'attività è noto per essere influenzato dal sito di iniezione, esercizio fisico e altre variabili (vedere Generale sotto PRECAUZIONI).
In uno studio sulla glicemia eseguito in 30 soggetti non diabetici, l'inizio dell'azione e l'attività ipoglicemizzante di Sono stati confrontati Humalog, Humalog® Mix50 / 50 ™, Humalog Mix75 / 25 e sospensione di insulina lispro protamina (componente NPL) (vedere Figura 2). I grafici della velocità media di infusione del glucosio rispetto al tempo hanno mostrato un profilo di attività insulinica distinto per ciascuna formulazione. La rapida insorgenza dell'attività ipoglicemizzante caratteristica di Humalog è stata mantenuta in Humalog Mix75 / 25.
In studi separati sul glucosio condotti su soggetti non diabetici, sono stati valutati la farmacodinamica di Humalog Mix75 / 25 e Humulin 70/30 e sono presentati nella Figura 3. Humalog Mix75 / 25 ha una durata di attività simile a quella di Humulin 70/30.
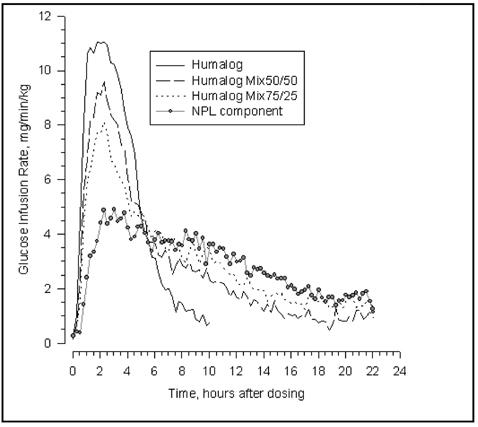
Figura 2: Attività insulinica dopo iniezione di Humalog, Humalog Mix50 / 50, Humalog Mix75 / 25 o sospensione di insulina Lispro Protamine (componente NPL) in 30 soggetti non diabetici.

Figura 3: Attività insulinica dopo iniezione di Humalog Mix75 / 25 e Humulin 70/30 in soggetti non diabetici.
Le figure 2 e 3 rappresentano i profili di attività dell'insulina misurati dagli studi sulla pinza del glucosio in soggetti sani non diabetici.
La Figura 2 mostra i profili di attività nel tempo di Humalog, Humalog Mix50 / 50, Humalog Mix75 / 25 e sospensione di insulina lispro protamina (componente NPL).
La Figura 3 è un confronto dei profili di attività nel tempo di Humalog Mix75 / 25 (vedi Figura 3a) e di Humulin 70/30 (vedi Figura 3b) da due diversi studi.
Popolazioni speciali
Età e Genere
Non sono disponibili informazioni sull'effetto dell'età sulla farmacocinetica di Humalog Mix75 / 25. I confronti farmacocinetici e farmacodinamici tra uomini e donne trattati con Humalog Mix75 / 25 non hanno mostrato differenze di genere. In ampi studi clinici su Humalog, l'analisi dei sottogruppi in base all'età e al sesso ha dimostrato che le differenze tra Humalog e insulina umana regolare nei parametri postprandiali del glucosio sono mantenuti trasversalmente sottogruppi.
fumo
L'effetto del fumo sulla farmacocinetica e farmacodinamica di Humalog Mix75 / 25 non è stato studiato.
Gravidanza
L'effetto della gravidanza sulla farmacocinetica e farmacodinamica di Humalog Mix75 / 25 non è stato studiato.
Obesità
L'effetto dell'obesità e / o dello spessore del grasso sottocutaneo sulla farmacocinetica e farmacodinamica di Humalog Mix75 / 25 non è stato studiato. In grandi studi clinici, che includevano pazienti con indice di massa corporea fino a 35 kg / m2 inclusi, n sono state osservate differenze coerenti tra Humalog e Humulin® R rispetto al glucosio postprandiale parametri.
Renale menomazione
L'effetto dell'insufficienza renale sulla farmacocinetica e farmacodinamica di Humalog Mix75 / 25 non è stato studiato. In uno studio su 25 pazienti con diabete di tipo 2 e un'ampia gamma di funzionalità renale, le differenze farmacocinetiche tra Humalog e insulina umana regolare sono state generalmente mantenute. Tuttavia, la sensibilità dei pazienti all'insulina è cambiata, con un aumento della risposta all'insulina con il declino della funzionalità renale. Nei pazienti con disfunzione renale può essere necessario un attento monitoraggio del glucosio e riduzioni della dose di insulina, incluso Humalog Mix75 / 25.
Insufficienza epatica
Alcuni studi con insulina umana hanno mostrato livelli aumentati di insulina circolante in pazienti con insufficienza epatica. L'effetto della compromissione epatica sulla farmacocinetica e farmacodinamica di Humalog Mix75 / 25 non è stato studiato. Tuttavia, in uno studio su 22 pazienti con diabete di tipo 2, la funzionalità epatica compromessa non ha influenzato la assorbimento sottocutaneo o disposizione generale di Humalog rispetto a pazienti senza anamnesi epatica disfunzione. In quello studio, Humalog ha mantenuto il suo assorbimento ed eliminazione più rapidi rispetto all'insulina umana regolare. Nei pazienti con disfunzione epatica può essere necessario un attento monitoraggio del glucosio e aggiustamenti della dose di insulina, incluso Humalog Mix75 / 25.
superiore
Indicazioni e utilizzo
Humalog Mix75 / 25, una miscela di 75% di sospensione di insulina lispro protamina e 25% di iniezione di insulina lispro, (origine di rDNA), è indicato nel trattamento di pazienti con diabete mellito per il controllo di iperglicemia. Humalog Mix75 / 25 ha un inizio più rapido dell'attività ipoglicemizzante rispetto a Humulin 70/30 pur avendo una durata d'azione simile. Questo profilo si ottiene combinando la rapida insorgenza di Humalog con l'azione intermedia della sospensione di insulina lispro protamina.
superiore
Controindicazioni
Humalog Mix75 / 25 è controindicato durante episodi di ipoglicemia e in pazienti sensibili all'insulina lispro o ad uno qualsiasi degli eccipienti contenuti nella formulazione.
superiore
Avvertenze
Humalog differisce dall'insulina umana regolare per la sua rapida insorgenza d'azione e per una durata più breve dell'attività. Pertanto, la dose di Humalog Mix75 / 25 deve essere somministrata entro 15 minuti prima di un pasto.
L'ipoglicemia è l'effetto avverso più comune associato all'uso di insuline, incluso Humalog Mix75 / 25. Come con tutte le insuline, i tempi dell'ipoglicemia possono differire tra le varie formulazioni di insulina. Il monitoraggio del glucosio è raccomandato per tutti i pazienti con diabete.
Qualsiasi cambiamento di insulina deve essere effettuato con cautela e solo sotto controllo medico. Cambiamenti nella concentrazione di insulina, produttore, tipo (ad es. Regular, NPH, analogo), specie o metodo di produzione possono comportare la necessità di un cambiamento nel dosaggio.
superiore
Precauzioni
Generale
L'ipoglicemia e l'ipopotassiemia sono tra i potenziali effetti avversi clinici associati all'uso di tutte le insuline. A causa delle differenze nell'azione di Humalog Mix75 / 25 e di altre insuline, si deve prestare attenzione nei pazienti in cui tali potenziali effetti collaterali potrebbero essere clinicamente rilevante (ad es. pazienti a digiuno, con neuropatia autonomica o che assumono farmaci per abbassare il potassio o pazienti che assumono farmaci sensibili al siero di potassio livello). La lipodistrofia e l'ipersensibilità sono tra gli altri potenziali effetti avversi clinici associati all'uso di tutte le insuline.
Come per tutte le preparazioni di insulina, il corso dell'azione di Humalog Mix75 / 25 può variare a seconda dei soggetti o in tempi diversi nello stesso individuo e dipende dal sito di iniezione, dall'afflusso di sangue, dalla temperatura e dal fisico attività.
L'adeguamento del dosaggio di qualsiasi insulina può essere necessario se i pazienti cambiano la loro attività fisica o il loro normale programma alimentare. Il fabbisogno di insulina può essere modificato durante malattie, disturbi emotivi o altri stress.
Ipoglicemia - Come per tutte le preparazioni di insulina, le reazioni ipoglicemizzanti possono essere associate alla somministrazione di Humalog Mix75 / 25. I rapidi cambiamenti nelle concentrazioni sieriche di glucosio possono indurre sintomi di ipoglicemia nelle persone con diabete, indipendentemente dal valore del glucosio. I sintomi di allarme precoce dell'ipoglicemia possono essere diversi o meno pronunciati in determinate condizioni, come ad es durata del diabete, patologie del nervo diabetico, uso di farmaci come i beta-bloccanti o diabete intensificato controllo.
Insufficienza renale - Come con altre insuline, i requisiti per Humalog Mix75 / 25 possono essere ridotti nei pazienti con insufficienza renale.
Insufficienza epatica - Sebbene la funzionalità epatica compromessa non influisca sull'assorbimento o sulla disposizione Humalog, un attento monitoraggio del glucosio e aggiustamenti della dose di insulina, incluso Humalog Mix75 / 25, possono essere necessario.
Allergia - Allergia locale - Come per qualsiasi terapia insulinica, i pazienti possono manifestare arrossamento, gonfiore o prurito nel sito di iniezione. Queste reazioni minori di solito si risolvono in pochi giorni o alcune settimane. In alcuni casi, queste reazioni possono essere correlate a fattori diversi dall'insulina, come irritanti nell'agente detergente per la pelle o scarsa tecnica di iniezione.
Allergia sistemica - Meno comune, ma potenzialmente più grave, è l'allergia generalizzata all'insulina, che può causare eruzione cutanea (incluso il prurito) su tutto il corpo, mancanza di respiro, respiro sibilante, riduzione della pressione sanguigna, polso rapido o sudorazione. I casi gravi di allergia generalizzata, inclusa la reazione anafilattica, possono essere potenzialmente letali. Sono state riportate reazioni localizzate e mialgie generalizzate con l'uso di cresolo come eccipiente iniettabile.
Produzione di anticorpi - Negli studi clinici, sono stati osservati anticorpi che reagiscono in modo crociato con insulina umana e insulina lispro in entrambi i gruppi di trattamento di miscele di insulina umana e insulina lispro.
Informazioni per i pazienti
I pazienti devono essere informati dei potenziali rischi e vantaggi di Humalog Mix75 / 25 e terapie alternative. I pazienti non devono miscelare Humalog Mix75 / 25 con qualsiasi altra insulina. Dovrebbero inoltre essere informati dell'importanza di una corretta conservazione dell'insulina, tecnica di iniezione, tempistica del dosaggio, aderenza alla pianificazione dei pasti, regolare attività fisica, monitoraggio regolare della glicemia, test periodici dell'emoglobina A1c, riconoscimento e gestione dell'ipo e dell'iperglicemia e valutazione periodica del diabete complicazioni.
I pazienti devono essere informati di informare il proprio medico se sono in gravidanza o se intendono rimanere incinta.
Riferire ai pazienti il foglio illustrativo per informazioni sull'aspetto normale, i tempi di somministrazione (entro 15 minuti prima di un pasto), la conservazione e gli effetti avversi comuni.
Per i pazienti che usano dispositivi per la somministrazione di penne per insulina: prima di iniziare la terapia, i pazienti devono leggere questo foglio illustrativo accompagna il prodotto farmaceutico e il Manuale dell'utente che accompagna il dispositivo di consegna e rileggere ogni volta che la prescrizione è rinnovato. I pazienti devono essere istruiti su come utilizzare correttamente il dispositivo di rilascio, adescare la penna in un flusso di insulina e smaltire correttamente gli aghi. I pazienti devono essere avvisati di non condividere le loro penne con gli altri.
Test di laboratorio
Come per tutte le insuline, la risposta terapeutica a Humalog Mix75 / 25 deve essere monitorata mediante test periodici della glicemia. Si raccomanda la misurazione periodica dell'emoglobina A1c per il monitoraggio del controllo glicemico a lungo termine.
superiore
Interazioni farmacologiche
Il fabbisogno di insulina può essere aumentato da farmaci con attività iperglicemica come corticosteroidi, isoniazide, alcuni farmaci ipolipemizzanti (ad es. niacina), estrogeni, contraccettivi orali, fenotiazine e sostituzione della tiroide terapia.
Il fabbisogno di insulina può essere ridotto in presenza di farmaci che aumentano la sensibilità all'insulina o hanno attività ipoglicemizzante, come quella orale agenti antidiabetici, salicilati, antibiotici sulfa, alcuni antidepressivi (inibitori della monoamino ossidasi), enzima di conversione dell'angiotensina inibitori, agenti bloccanti del recettore dell'angiotensina II, bloccanti beta-adrenergici, inibitori della funzione pancreatica (ad es. octreotide) e alcool. I bloccanti beta-adrenergici possono mascherare i sintomi dell'ipoglicemia in alcuni pazienti.
Cancerogenesi, mutagenesi, alterazione della fertilità
Non sono stati condotti studi a lungo termine su animali per valutare il potenziale cancerogeno di Humalog, Humalog Mix75 / 25 o Humalog Mix50 / 50. L'insulina lispro non è risultata mutagena in una serie di test di tossicità genetica in vitro e in vivo (batterica test di mutazione, sintesi del DNA non programmata, test del linfoma del topo, test di aberrazione cromosomica e test del micronucleo). Non ci sono prove da studi su animali di compromissione della fertilità indotta dall'insulina lispro.
Gravidanza
Effetti teratogeni - Gravidanza Categoria B
Studi sulla riproduzione con insulina lispro sono stati condotti su ratti e conigli in gravidanza a livello parenterale dosi fino a 4 e 0,3 volte, rispettivamente, la dose media umana (40 unità / giorno) in base alla superficie corporea la zona. I risultati non hanno rivelato alcuna evidenza di ridotta fertilità o danno al feto a causa dell'insulina lispro. Tuttavia, non esistono studi adeguati e ben controllati con Humalog, Humalog Mix75 / 25 o Humalog Mix50 / 50 in donne in gravidanza. Poiché gli studi sulla riproduzione animale non sono sempre predittivi della risposta umana, questo farmaco deve essere usato durante la gravidanza solo se chiaramente necessario.
Madri che allattano
Non è noto se l'insulina lispro sia escreta in quantità significative nel latte materno. Molti farmaci, compresa l'insulina umana, vengono escreti nel latte materno. Per questo motivo, si deve usare cautela quando Humalog Mix75 / 25 viene somministrato a una donna che allatta. I pazienti con diabete che stanno allattando possono richiedere aggiustamenti della dose di Humalog Mix75/25, del piano alimentare o di entrambi.
Uso pediatrico
La sicurezza e l'efficacia di Humalog Mix75 / 25 nei pazienti di età inferiore ai 18 anni non sono state stabilite.
Uso geriatrico
Gli studi clinici su Humalog Mix75 / 25 non hanno incluso un numero sufficiente di pazienti di età pari o superiore a 65 anni per determinare se rispondono in modo diverso rispetto ai pazienti più giovani. In generale, la selezione della dose per un paziente anziano deve prendere in considerazione la maggiore frequenza di riduzione della funzionalità epatica, renale o cardiaca e di concomitante malattia o altra terapia farmacologica in questo popolazione.
superiore
Reazioni avverse
Gli studi clinici che hanno confrontato Humalog Mix75 / 25 con miscele di insulina umana non hanno dimostrato una differenza nella frequenza degli eventi avversi tra i due trattamenti.
Gli eventi avversi comunemente associati alla terapia insulinica umana comprendono:
Corpo nel suo insieme - reazioni allergiche (vedi PRECAUZIONI).
Pelle e appendici - reazione nel sito di iniezione, lipodistrofia, prurito, eruzione cutanea.
Altro - ipoglicemia (vedi AVVERTENZE e PRECAUZIONI).
superiore
Overdose
L'ipoglicemia può verificarsi a causa di un eccesso di insulina rispetto all'assunzione di cibo, al dispendio energetico o ad entrambi. Lievi episodi di ipoglicemia di solito possono essere trattati con glucosio orale. Potrebbero essere necessari aggiustamenti del dosaggio del farmaco, dei modelli di pasto o dell'esercizio fisico. Gli episodi più gravi con coma, convulsioni o danno neurologico possono essere trattati con glucagone intramuscolare / sottocutaneo o glucosio endovenoso concentrato. L'assunzione e l'osservazione sostenute di carboidrati possono essere necessarie perché l'ipoglicemia può ripresentarsi dopo un evidente recupero clinico
superiore
Dosaggio e amministrazione
Tabella 1 *: Riepilogo delle proprietà farmacodinamiche dei prodotti insulinici (confronto incrociato di studi incrociati)
| |||
Prodotti insulinici |
Dose, U / kg |
Tempo di picco dell'attività, ore dopo il dosaggio |
Percentuale dell'attività totale che si verifica nelle prime 4 ore |
Humalog |
0.3 |
2.4 |
70% |
Humulin R |
0.32 |
4.4 |
54% |
Humalog Mix75 / 25 |
0.3 |
2.6 |
35% |
Humulin 70/30 |
0.3 |
4.4 |
32% |
Humalog Mix50 / 50 |
0.3 |
2.3 |
45% |
Humulin 50/50 |
0.3 |
3.3 |
44% |
NPH |
0.32 |
5.5 |
14% |
Componente NPL |
0.3 |
5.8 |
22% |
Humalog Mix75 / 25 è destinato esclusivamente alla somministrazione sottocutanea. Humalog Mix75 / 25 non deve essere somministrato per via endovenosa. I regimi di dosaggio di Humalog Mix75 / 25 variano tra i pazienti e devono essere determinati dal operatore sanitario che abbia familiarità con i bisogni metabolici del paziente, le abitudini alimentari e altri stili di vita variabili. Humalog ha dimostrato di essere equipotente all'insulina umana regolare su base molare. Un'unità di Humalog ha lo stesso effetto ipoglicemizzante di un'unità di insulina umana regolare, ma il suo effetto è più rapido e di durata più breve. Humalog Mix75 / 25 ha un effetto ipoglicemizzante simile rispetto a Humulin 70/30 su un'unità per unità di base. Il più rapido effetto ipoglicemizzante di Humalog è correlato al più rapido tasso di assorbimento dell'insulina lispro dal tessuto sottocutaneo.
Humalog Mix75 / 25 inizia a ridurre la glicemia più rapidamente dell'insulina umana regolare, consentendo un dosaggio conveniente immediatamente prima di un pasto (entro 15 minuti). Al contrario, le miscele contenenti insulina umana regolare devono essere somministrate da 30 a 60 minuti prima di un pasto.
Il tasso di assorbimento di insulina e di conseguenza l'inizio dell'attività sono noti per essere influenzati dal sito di iniezione, esercizio fisico e altre variabili. Come per tutte le preparazioni di insulina, il corso d'azione di Humalog Mix75 / 25 può variare considerevolmente in soggetti diversi o all'interno dello stesso individuo. I pazienti devono essere istruiti a utilizzare le tecniche di iniezione appropriate.
Humalog Mix75 / 25 deve essere ispezionato visivamente prima dell'uso. Humalog Mix75 / 25 deve essere usato solo se appare uniformemente torbido dopo la miscelazione. Humalog Mix75 / 25 non deve essere usato dopo la data di scadenza.
superiore
Come fornito
Humalog Mix75 / 25 [75% di sospensione di insulina lispro protamina e 25% di iniezione di insulina lispro, (origine rDNA)] è disponibile nelle seguenti confezioni: ogni presentazione contiene 100 unità di insulina lispro per ml (U-100).
Flaconcini da 10 ml |
NDC 0002-7511-01 (VL-7511) |
5 x 3 mL di dispositivi per la somministrazione di insulina preriempita (penna) |
NDC 0002-8794-59 (HP-8794) |
5 dispositivi di erogazione di insulina preriempiti da 3 ml (KwikPen ™) |
NDC 0002-8797-59 (HP-8797) |
Conservazione - Humalog Mix75 / 25 deve essere conservato in frigorifero [da 2 ° a 8 ° C (36 ° a 46 ° F)], ma non nel congelatore. Non utilizzare Humalog Mix75 / 25 se è stato congelato. I flaconcini non refrigerati [inferiori a 30 ° C (86 ° F)] devono essere utilizzati entro 28 giorni o eliminati, anche se contengono ancora Humalog Mix75 / 25. Penne non refrigerate [inferiori a 30 ° C (86 ° F)] e penne Kwik devono essere utilizzate entro 10 giorni o eliminate, anche se contengono Humalog Mix75 / 25. Proteggere dal calore e dalla luce diretti. Vedi tabella sotto:
Temperatura ambiente non in uso (non aperta) [inferiore a 30 ° C (86 ° F)] |
Non in uso (non aperto) refrigerato |
Temperatura ambiente (aperta) in uso [inferiore a 30 ° C (86 ° F)] |
|
Flaconcino da 10 ml |
28 giorni |
Fino alla data di scadenza |
28 giorni, refrigerato / temperatura ambiente. |
Penna da 3 ml e KwikPen (preriempita) |
10 giorni |
Fino alla data di scadenza |
10 giorni. Non refrigerare. |
KwikPens prodotto da Eli Lilly and Company, Indianapolis, IN 46285, USA
Penne prodotte da Eli Lilly and Company, Indianapolis, IN 46285, USA o Lilly France, F-67640 Fegersheim, Francia
Fiale prodotte da Eli Lilly and Company, Indianapolis, IN 46285, USA o Lilly France, F-67640 Fegersheim, Francia per Eli Lilly and Company, Indianapolis, IN 46285, USA
www. Humalog.com
PV 5551 AMP
ultimo aggiornamento 03/2009
Humalog Pen, Humalog Cartridge, KwikPen, informazioni sul paziente insulina lispro (in inglese semplice)
Informazioni dettagliate su segni, sintomi, cause, trattamenti del diabete
Le informazioni contenute in questa monografia non intendono coprire tutti i possibili usi, indicazioni, precauzioni, interazioni farmacologiche o effetti avversi. Questa informazione è generalizzata e non è intesa come consulenza medica specifica. Se ha domande sui medicinali che sta assumendo o desidera ulteriori informazioni, consultare il medico, il farmacista o l'infermiere.
torna a: Sfoglia tutti i farmaci per il diabete



