Byetta per il trattamento del diabete
Marchio: Byetta
Nome generico: Exenatide
Forma di dosaggio: iniezione
Contenuti:
Descrizione
Farmacologia clinica
Studi clinici
Indicazioni e utilizzo
Controindicazioni
Precauzioni
Reazioni avverse
sovradosaggio
Dosaggio e amministrazione
Conservazione
Come fornito
Byetta (Exenatide) Informazioni paziente (in inglese semplice)
Descrizione
Byetta® (exenatide) è un peptide sintetico che ha azioni incretine-mimetiche ed è stato originariamente identificato nella lucertola Heloderma suspectum. Byetta migliora la secrezione di insulina glucosio-dipendente da parte delle cellule beta del pancreas, sopprime la secrezione di glucagone in modo inappropriato e rallenta lo svuotamento gastrico. Exenatide differisce nella struttura chimica e nell'azione farmacologica da insulina, sulfoniluree (incluso Derivati della D-fenilalanina e meglitinidi), biguanidi, tiazolidinedioni e alfa-glucosidasi inibitori.
Exenatide è un'ammide peptide amminoacidica. Exenatide ha la formula empirica C184H282N50O60S e peso molecolare di 4186,6 Dalton. La sequenza di aminoacidi per exenatide è mostrata di seguito.
H - His - Gly - Glu - Gly - Thr - Phe - Thr - Ser - Asp - Leu - Ser - Lys - Gln - Met - Glu - Glu - Glu - Ala - Val - Arg - Leu - Phe - Ile - Glu - Trp - Leu - Lys - Asn - Gly - Gly - Pro - Ser - Ser - Gly - Ala - Pro - Pro - Pro - Ser - NH2
Byetta viene fornito per l'iniezione sottocutanea (SC) come soluzione isotonica sterile conservata in una cartuccia di vetro che è stata assemblata in un iniettore-penna (penna). Ogni millilitro (mL) contiene 250 microgrammi (mcg) di exenatide sintetico, 2,2 mg di metacresolo come conservante antimicrobico, mannitolo come agente di regolazione della tonicità e acido acetico glaciale e acetato di sodio triidrato in acqua per preparazioni iniettabili come soluzione tampone a pH 4,5. Sono disponibili due penne preriempite per erogare dosi unitarie di 5 mcg o 10 mcg. Ogni penna preriempita erogherà 60 dosi per fornire 30 giorni di somministrazione due volte al giorno (BID).
superiore
Farmacologia clinica
Meccanismo di azione
Le incretine, come il peptide-1 glucagonico (GLP-1), aumentano la secrezione di insulina glucosio-dipendente e mostrano altre azioni anti-iperglicemiche a seguito del loro rilascio nella circolazione dall'intestino. Exenatide è un agente mimetico di incretina che imita il potenziamento della secrezione di insulina glucosio-dipendente e diverse altre azioni antiiperglicemiche delle incretine.
La sequenza aminoacidica di exenatide si sovrappone parzialmente a quella del GLP-1 umano. Exenatide ha dimostrato di legare e attivare il recettore GLP-1 umano noto in vitro. Ciò porta ad un aumento della sintesi insulino-dipendente del glucosio e della secrezione in vivo di insulina da cellule beta del pancreas, mediante meccanismi che coinvolgono AMP ciclico e / o altri segnali intracellulari percorsi. Exenatide promuove il rilascio di insulina dalle cellule beta in presenza di elevate concentrazioni di glucosio. Quando somministrato in vivo, exenatide imita alcune azioni antiiperglicemiche del GLP-1.
Byetta migliora il controllo glicemico riducendo le concentrazioni di glucosio a digiuno e postprandiale nei pazienti con diabete di tipo 2 attraverso le azioni descritte di seguito.
Secrezione di insulina glucosio-dipendente: Byetta ha effetti acuti sulla reattività delle cellule beta del pancreas al glucosio e porta al rilascio di insulina solo in presenza di elevate concentrazioni di glucosio. Questa secrezione di insulina si attenua man mano che le concentrazioni di glucosio nel sangue diminuiscono e si avvicinano all'euglicemia.
Risposta insulinica della prima fase: in soggetti sani, si verifica una forte secrezione di insulina durante i primi 10 minuti dopo la somministrazione endovenosa di glucosio (IV). Questa secrezione, nota come "risposta insulinica di prima fase", è tipicamente assente nei pazienti con diabete di tipo 2. La perdita della risposta insulinica di prima fase è un difetto precoce delle cellule beta nel diabete di tipo 2. La somministrazione di Byetta a concentrazioni plasmatiche terapeutiche ha ripristinato la risposta insulinica di prima fase a un bolo IV di glucosio nei pazienti con diabete di tipo 2 (Figura 1). Sia la secrezione di insulina di prima fase che la secrezione di insulina di seconda fase erano significativamente aumentate nei pazienti con diabete di tipo 2 trattati con Byetta rispetto alla soluzione salina (p
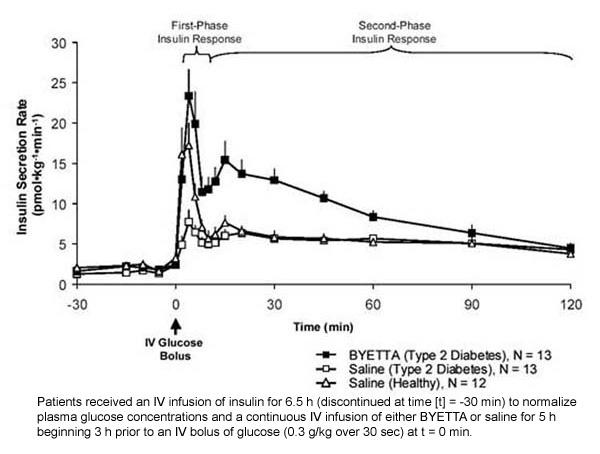
Figura 1: Tasso di secrezione media (+ SEM) di insulina durante l'infusione di Byetta o soluzione salina in pazienti con diabete di tipo 2 e durante l'infusione di soluzione salina in soggetti sani
Secrezione di glucagone: nei pazienti con diabete di tipo 2, Byetta modera la secrezione di glucagone e riduce le concentrazioni sieriche di glucagone durante i periodi di iperglicemia. Concentrazioni più basse di glucagone portano a una riduzione della produzione di glucosio epatico e una riduzione della domanda di insulina. Tuttavia, Byetta non altera la normale risposta del glucagone all'ipoglicemia.
Svuotamento gastrico: Byetta rallenta lo svuotamento gastrico, riducendo in tal modo la velocità con cui il glucosio derivato dal pasto appare nella circolazione.
Assunzione di cibo: sia negli animali che nell'uomo, la somministrazione di exenatide ha dimostrato di ridurre l'assunzione di cibo.
farmacocinetica
Assorbimento
Dopo la somministrazione di SC a pazienti con diabete di tipo 2, exenatide raggiunge le concentrazioni plasmatiche di picco mediane in 2,1 ore. Picco medio di concentrazione di exenatide (Cmax) era 211 pg / mL e l'area media complessiva sotto la curva (AUC0-inf) era 1036 pg-h / mL a seguito della somministrazione di SC di una dose di 10 mcg di Byetta. L'esposizione a exenatide (AUC) è aumentata proporzionalmente nell'intervallo di dosi terapeutiche da 5 mcg a 10 mcg. I valori di Cmax sono aumentati meno che proporzionalmente nello stesso intervallo. Un'esposizione simile si ottiene con la somministrazione SC di Byetta nell'addome, nella coscia o nel braccio.
Distribuzione
Il volume apparente medio di distribuzione di exenatide dopo somministrazione di SC di una singola dose di Byetta è di 28,3 L.
Metabolismo ed eliminazione
Studi non clinici hanno dimostrato che exenatide viene principalmente eliminata mediante filtrazione glomerulare con conseguente degradazione proteolitica. La clearance apparente media di exenatide nell'uomo è di 9,1 L / he l'emivita terminale media è di 2,4 ore. Queste caratteristiche farmacocinetiche di exenatide sono indipendenti dalla dose. Nella maggior parte degli individui, le concentrazioni di exenatide sono misurabili per circa 10 ore dopo la dose.
Popolazioni speciali
Insufficienza renale
Nei pazienti con insufficienza renale da lieve a moderata (clearance della creatinina da 30 a 80 mL / min), la clearance dell'exenatide è stata solo lievemente ridotta; pertanto, nei pazienti con insufficienza renale da lieve a moderata non è necessario alcun aggiustamento della dose di Byetta. Tuttavia, nei pazienti con malattia renale allo stadio terminale sottoposti a dialisi, la clearance media di exenatide è ridotta a 0,9 L / h rispetto a 9,1 L / h in soggetti sani (vedere PRECAUZIONI, Generale).
Insufficienza epatica
Non sono stati condotti studi di farmacocinetica in pazienti con diagnosi di insufficienza epatica acuta o cronica. Poiché exenatide è eliminato principalmente dal rene, non si prevede che la disfunzione epatica influenzi le concentrazioni ematiche di exenatide (vedere farmacocinetica, Metabolismo ed eliminazione).
geriatrico
L'analisi farmacocinetica di popolazione dei pazienti (range da 22 a 73 anni) suggerisce che l'età non influenza le proprietà farmacocinetiche di exenatide.
pediatrico
Exenatide non è stato studiato in pazienti pediatrici.
Genere
L'analisi farmacocinetica di popolazione su pazienti maschi e femmine suggerisce che il genere non influenza la distribuzione e l'eliminazione di exenatide.
Gara
L'analisi farmacocinetica di popolazione su pazienti inclusi Caucasico, Ispanico e Nero, suggerisce che la razza non ha un'influenza significativa sulla farmacocinetica di exenatide.
Obesità
L'analisi farmacocinetica di popolazione di pazienti obesi (BMI - 30 kg / m2) e non obesi suggerisce che l'obesità non ha effetti significativi sulla farmacocinetica di exenatide.
Interazioni farmacologiche
digossina
La somministrazione concomitante di dosi ripetute di Byetta (10 mcg di BID) ha ridotto la Cmax di digossina orale (0,25 mg QD) del 17% e ritardato la Tmax di circa 2,5 ore; tuttavia, l'esposizione farmacocinetica (AUC) allo stato stazionario complessivo non è stata modificata.
lovastatina
L'AUC e la Cmax della lovastatina sono diminuite rispettivamente del 40% e del 28% circa e la Tmax è stata ritardata di circa 4 ore quando Byetta (10 mcg BID) è stato somministrato in concomitanza con una singola dose di lovastatina (40 mg) rispetto alla lovastatina somministrata solo. Negli studi clinici controllati della durata di 30 settimane di Byetta, l'uso di Byetta in pazienti già trattati con HMG Gli inibitori della CoA reduttasi non sono stati associati a cambiamenti coerenti nei profili lipidici rispetto a basale.
Lisinopril
Nei pazienti con ipertensione da lieve a moderata stabilizzata su lisinopril (da 5 a 20 mg / die), Byetta (10 mcg BID) non ha alterato la Cmax o l'AUC allo stato stazionario di lisinopril. Lisinopril a stato stazionario Tmax è stato ritardato di 2 ore. Non ci sono stati cambiamenti nella pressione sanguigna sistolica e diastolica media su 24 ore.
acetaminofene
Quando sono stati somministrati 1000 mg di elisir di paracetamolo con 10 mcg di Byetta (0 ore) e 1 ora, 2 ore e 4 ore dopo l'iniezione di Byetta, gli AUC di acetaminofene sono diminuiti del 21%, 23%, 24% e 14%, rispettivamente; Cmax è stato ridotto del 37%, 56%, 54% e 41%, rispettivamente; Tmax è stato aumentato da 0,6 ore nel periodo di controllo a 0,9 ore, 4,2 ore, 3,3 ore e 1,6 ore, rispettivamente. Paracetamolo AUC, Cmax e Tmax non sono stati significativamente modificati quando il paracetamolo è stato somministrato 1 ora prima dell'iniezione di Byetta.
warfarin
Somministrazione concomitante di dosi ripetute di Byetta (5 mcg di BID nei giorni 1-2 e 10 mcg di BID nei giorni 3-9) in volontari sani, ritardo di warfarin (25 mg) di Tmax di circa 2 ore. Non sono stati osservati effetti clinicamente rilevanti sulla Cmax o sull'AUC degli enantiomeri S e R del warfarin. Byetta non ha modificato le proprietà farmacodinamiche (come valutato dalla risposta INR) del warfarin.
farmacodinamica
Glucosio postprandiale
Nei pazienti con diabete di tipo 2, Byetta riduce le concentrazioni postprandiali di glucosio plasmatico (Figura 2).

figura 2: Media (+ SEM) Concentrazioni plasmatiche postprandiali di glucosio nel primo giorno di Byettaun' Trattamento in pazienti con diabete di tipo 2 trattati con metformina, una sulfonilurea o entrambi (N = 54)
Glicemia a digiuno
In uno studio crossover monodose in pazienti con diabete di tipo 2 e iperglicemia a digiuno, un rilascio immediato di insulina ha seguito l'iniezione di Byetta. Le concentrazioni plasmatiche di glucosio sono state significativamente ridotte con Byetta rispetto al placebo (Figura 3).

Figura 3: Concentrazioni sieriche medie (+ SEM) di insulina e glucosio plasmatico a seguito di un'iniezione singola di Byettaun' o placebo in pazienti a digiuno con diabete di tipo 2 (N = 12)
superiore
Studi clinici
Utilizzare con metformina e / o una sulfonilurea
Sono stati condotti tre studi di 30 settimane, in doppio cieco, controllati con placebo per valutare la sicurezza e l'efficacia di Byetta in pazienti con tipo 2 diabete il cui controllo glicemico era inadeguato con la sola metformina, una sola sulfonilurea o la metformina in associazione con un sulfonilurea.
Un totale di 1446 pazienti sono stati randomizzati in questi tre studi: 991 (68,5%) erano caucasici, 224 (15,5%) erano ispanici e 174 (12,0%) erano neri. I valori medi di HbA1c al basale per gli studi variavano dall'8,2% all'8,7%. Dopo un periodo iniziale di placebo di 4 settimane, i pazienti sono stati assegnati in modo casuale a ricevere Byetta 5 mcg BID, Byetta 10 mcg BID o BID placebo prima dei pasti del mattino e della sera, oltre al loro antidiabetico orale esistente agente. Tutti i pazienti assegnati a Byetta hanno iniziato un periodo di inizio del trattamento con 5 mcg di BID per 4 settimane. Dopo 4 settimane, quei pazienti hanno continuato a ricevere Byetta 5 mcg BID o la loro dose è stata aumentata a 10 mcg BID. I pazienti assegnati al placebo hanno ricevuto BID placebo durante lo studio.
L'endpoint primario in ogni studio era il cambiamento medio rispetto all'HbA basale1c a 30 settimane. I risultati dello studio di trenta settimane sono riassunti nella Tabella 1.
Tabella 1: Risultati di trenta settimane di placebo controllati con placebo di Byetta in pazienti con insufficiente controllo del glucosio nonostante l'uso di metformina, una sulfonilurea o entrambi
| Placebo OFFERTA |
Byetta 5 mcg BID |
Byetta 10 mcg* OFFERTA |
|
|---|---|---|---|
| |||
| In combinazione con metformina | |||
| Popolazione intent-to-treat (N) | 113 | 110 | 113 |
| HbA1c (%), Significare | |||
| Baseline | 8.2 | 8.3 | 8.2 |
| Modifica alla settimana 30 | +0.1 | −0.4†| −0.8c |
| Proporzione Raggiungimento dell'HbA1c≤7% § | 13.0% | 31.6%†| 46.4%†|
| Peso corporeo (kg), media | |||
| Baseline | 99.9 | 100.0 | 100.9 |
| Modifica alla settimana 30 | −0.3 | −1.6†| −2.8c |
| In combinazione con una sulfonilurea | |||
| Popolazione intent-to-treat (N) | 123 | 125 | 129 |
| HbA1c (%), Significare | |||
| Baseline | 8.7 | 8.5 | 8.6 |
| Modifica alla settimana 30 | +0.1 | −0.5†| −0.9c |
| Proporzione Raggiungimento dell'HbA1c≤7% § | 8.8% | 32.6%†| 41.3%c |
| Peso corporeo (kg), media | |||
| Baseline | 99.1 | 94.9 | 95.2 |
| Modifica alla settimana 30 | −0.6 | −0.9 | −1.6†|
| In combinazione con metformina e una sulfonilurea | |||
| Popolazione intent-to-treat (N) | 247 | 245 | 241 |
| HbA1c (%), Significare | |||
| Baseline | 8.5 | 8.5 | 8.5 |
| Modifica alla settimana 30 | +0.2 | −0.6c | −0.8c |
| Proporzione Raggiungimento dell'HbA1c≤7% § | 9.2% | 27.4%c | 33.5%c |
| Peso corporeo (kg), media | |||
| Baseline | 99.1 | 96.9 | 98.4 |
| Modifica alla settimana 30 | −0.9 | −1.6†| −1.6†|
HbA1c
L'aggiunta di Byetta a un regime di metformina, una sulfonilurea o entrambi, ha determinato riduzioni statisticamente significative dall'HbA al basale1c alla settimana 30 rispetto ai pazienti trattati con placebo aggiunti a questi agenti nei tre studi controllati (Tabella 1). Inoltre, è stato osservato un effetto dose-statisticamente significativo tra i gruppi Byetta da 5 mcg e 10 mcg per la variazione dall'HbA basale1c alla settimana 30 nei tre studi.
Glucosio a digiuno e postprandiale
L'uso a lungo termine di Byetta in combinazione con metformina, una sulfonilurea o entrambi, ha ridotto sia il digiuno che concentrazioni di glucosio plasmatico postprandiale in modo statisticamente significativo, dose-dipendente per tutta la settimana 30. Una riduzione statisticamente significativa rispetto al basale delle concentrazioni di glucosio sia a digiuno che postprandiali è stato osservato alla settimana 30 in entrambi i gruppi Byetta rispetto al placebo nei dati combinati dei tre controllati prove. La variazione della concentrazione di glucosio a digiuno alla settimana 30 rispetto al basale era di 88 mg / dL per Byetta 5 mcg BID e di 1010 mg / dL per Byetta 10 mcg BID, rispetto a +12 mg / dL per il placebo. La variazione della concentrazione di glucosio postprandiale dopo 2 ore dalla somministrazione di Byetta alla settimana 30 è stata confrontata con basale era di 6363 mg / dL per 5 mcg di BID e di ˆ71 mg / dL per 10 mcg di BID, rispetto a +11 mg / dL per placebo.
Proporzione di pazienti che ottengono HbA1c≤7%
Byetta in combinazione con metformina, una sulfonilurea o entrambi, ha determinato un maggiore statisticamente significativo percentuale di pazienti che ottengono un HbA1câ € 7% alla settimana 30 rispetto ai pazienti che assumono placebo in associazione con questi agenti (Tabella 1).
Peso corporeo
Nei tre studi controllati, una riduzione dal peso corporeo basale alla settimana 30 è stata associata a BID Byetta 10 mcg rispetto al BID placebo nei pazienti con diabete di tipo 2 (Tabella 1).
Risultati clinici di un anno
La coorte di 163 pazienti degli studi controllati verso placebo della durata di 30 settimane che hanno completato un totale di 52 settimane di trattamento con Byetta 10 mcg BID ha mostrato variazioni di HbA1c rispetto al basale del "1,0% e" 1,1% a 30 e 52 settimane di trattamento, rispettivamente, con variazioni di accompagnamento rispetto al basale della glicemia a digiuno di "14,0 mg / dL e" 25,3 mg / dL e variazioni del peso corporeo di "2,6 kg e" 3,6 " kg. Questa coorte aveva valori basali simili a quelli dell'intera popolazione di studi controllati.
Utilizzare con un tiazolidinedione
In uno studio randomizzato, in doppio cieco, controllato con placebo della durata di 16 settimane, Byetta (n = 121) o placebo (n = 112) sono stati aggiunti a quelli esistenti trattamento con tiazolidinedione (pioglitazone o rosiglitazone), con o senza metformina, in pazienti con diabete di tipo 2 con inadeguata controllo glicemico. La randomizzazione con Byetta o placebo è stata stratificata in base al fatto che i pazienti stessero ricevendo metformina. I pazienti assegnati al placebo hanno ricevuto BID placebo durante lo studio. Byetta o placebo sono stati iniettati per via sottocutanea prima dei pasti del mattino e della sera. Il 77% dei pazienti stava assumendo un tiazolidinedione e metformina e il 21% stava assumendo un tiazolidinedione da solo. La maggior parte dei pazienti (84%) era caucasica, l'8% era ispanica e il 3% era nera. I valori medi basali di HbA1c erano simili per Byetta e placebo (7,9%). Il trattamento con Byetta è stato iniziato alla dose di 5 mcg di BID per 4 settimane, quindi aumentato a 10 mcg di BID per altre 12 settimane.
I risultati dello studio di sedici settimane sono riassunti nella Tabella 2. Rispetto al placebo, Byetta ha comportato riduzioni statisticamente significative dell'HbA1c rispetto al basale alla Settimana 16. Gli effetti del trattamento per HbA1c erano simili nei due sottogruppi definiti dallo strato di trattamento sottostante (tiazolidinedioni da soli contro tiazolidinedioni più metformina). La variazione della concentrazione di glucosio nel siero a digiuno dal basale alla Settimana 16 è stata statisticamente significativa rispetto al placebo (2121 mg / dL per Byetta 10 mcg BID rispetto a +4 mg / dL per il placebo).
Tabella 2: risultati di una sperimentazione controllata da placebo di 16 settimane di Byetta in pazienti con insufficiente controllo del glucosio nonostante l'uso di un tiazolidinedione (TZD) o di un tiazolidinedione più metformina
| Placebo OFFERTA |
Byetta 10 mcg* OFFERTA |
|
|---|---|---|
| ||
| In combinazione con un TZD o un TZD più MET | ||
| Popolazione intent-to-treat (N) | 112 | 121 |
| HbA1c (%), Significare | ||
| Baseline | 7.9 | 7.9 |
| Modifica alla settimana 16 | +0.1 | −0.8†|
| Proporzione Raggiungimento dell'HbA1c≤7%c | 16.2% | 62.3%†|
| Peso corporeo (kg), media | ||
| Baseline | 96.9 | 97.5 |
| Modifica alla settimana 16 | −0.2 | −1.5†|
superiore
Indicazioni e utilizzo
Byetta è indicato come terapia aggiuntiva per migliorare il controllo glicemico nei pazienti con diabete mellito di tipo 2 che assumono metformina, una sulfonilurea, un tiazolidinedione, una combinazione di metformina e una sulfonilurea, o una combinazione di metformina e un tiazolidinedione, ma non hanno raggiunto un'adeguata glicemia controllo.
superiore
Controindicazioni
Byetta è controindicato in pazienti con nota ipersensibilità a exenatide o ad uno qualsiasi dei componenti del prodotto.
superiore
Precauzioni
Generale
Byetta non sostituisce l'insulina nei pazienti che richiedono insulina. Byetta non deve essere usato in pazienti con diabete di tipo 1 o per il trattamento della chetoacidosi diabetica.
I pazienti possono sviluppare anticorpi anti-exenatide dopo il trattamento con Byetta, coerentemente con le proprietà potenzialmente immunogene dei farmaci proteici e peptidici. I pazienti che ricevono Byetta devono essere osservati per segni e sintomi di reazioni di ipersensibilità.
In una piccola percentuale di pazienti, la formazione di anticorpi anti-exenatide ad alto titolo potrebbe comportare il mancato raggiungimento di un adeguato miglioramento del controllo glicemico. In caso di peggioramento del controllo glicemico o mancato raggiungimento del controllo glicemico mirato, si deve prendere in considerazione una terapia antidiabetica alternativa.
L'uso concomitante di Byetta con insulina, derivati della D-fenilalanina, meglitinidi o inibitori dell'alfa-glucosidasi non è stato studiato.
Byetta non è raccomandato per l'uso in pazienti con malattia renale allo stadio terminale o grave insufficienza renale (farmacocinetica di clearance della creatinina, popolazioni speciali). Nei pazienti con malattia renale allo stadio terminale sottoposti a dialisi, dosi singole di Byetta 5 mcg non sono state ben tollerate a causa degli effetti collaterali gastrointestinali.
Ci sono stati eventi rari, segnalati spontaneamente di alterata funzionalità renale, incluso aumento del siero creatinina, insufficienza renale, peggioramento dell'insufficienza renale cronica e insufficienza renale acuta, che a volte richiedono emodialisi. Alcuni di questi eventi si sono verificati in pazienti in trattamento con uno o più agenti farmacologici noti per influire sulla funzionalità renale stato della funzione / idratazione e / o in pazienti con nausea, vomito e / o diarrea, con o senza disidratazione. Gli agenti concomitanti includevano inibitori dell'enzima di conversione dell'angiotensina, farmaci antinfiammatori non steroidei e diuretici. È stata osservata reversibilità della funzionalità renale alterata con il trattamento di supporto e l'interruzione di agenti potenzialmente causali, incluso exenatide. Exenatide non è stato trovato per essere direttamente nefrotossico in studi preclinici o clinici.
Byetta non è stato studiato in pazienti con grave malattia gastrointestinale, inclusa la gastroparesi. Il suo uso è comunemente associato a effetti avversi gastrointestinali, tra cui nausea, vomito e diarrea. Pertanto, l'uso di Byetta non è raccomandato nei pazienti con grave malattia gastrointestinale. Lo sviluppo di un forte dolore addominale in un paziente trattato con Byetta deve essere studiato perché potrebbe essere un segnale di avvertimento di una condizione grave.
L'ipoglicemia
Negli studi clinici controllati della durata di 30 settimane con Byetta, un episodio di ipoglicemia è stato registrato come evento avverso se il paziente ha riportato sintomi associati a ipoglicemia con un accompagnamento di glicemia DOSAGGIO E AMMINISTRAZIONE).
Tabella 3: Incidenza (%) di ipoglicemia * mediante terapia antidiabetica concomitante
| Byetta | Byetta | Byetta | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Placebo OFFERTA |
5 mcg OFFERTA |
10 mcg OFFERTA |
Placebo OFFERTA |
5 mcg OFFERTA |
10 mcg OFFERTA |
Placebo OFFERTA |
5 mcg OFFERTA |
10 mcg OFFERTA |
|
| Con Metformina | Con una solfonilurea | Con MET / SFU | |||||||
| Byetta e placebo sono stati somministrati prima dei pasti del mattino e della sera. | |||||||||
| Abbreviazioni: BID, due volte al giorno; MET / SFU, metformina e una sulfonilurea. | |||||||||
| |||||||||
| N | 113 | 110 | 113 | 123 | 125 | 129 | 247 | 245 | 241 |
| L'ipoglicemia | 5.3% | 4.5% | 5.3% | 3.3% | 14.4% | 35.7% | 12.6% | 19.2% | 27.8% |
Quando usato come componente aggiuntivo di un tiazolidinedione, con o senza metformina, l'incidenza di ipoglicemia sintomatica da lieve a moderata con Byetta è stata dell'11% rispetto al 7% con placebo.
Byetta non ha modificato le risposte ormonali controregolatorie all'ipoglicemia indotta da insulina in uno studio randomizzato, in doppio cieco, controllato su soggetti sani.
Informazioni per i pazienti
I pazienti devono essere informati dei potenziali rischi di Byetta. I pazienti devono inoltre essere pienamente informati sulle pratiche di autogestione, inclusa l'importanza di una corretta conservazione di Byetta, iniezione tecnica, tempistica del dosaggio di Byetta e concomitanti farmaci orali, aderenza alla pianificazione dei pasti, attività fisica regolare, periodica monitoraggio della glicemia e test dell'HbA1c, riconoscimento e gestione dell'ipoglicemia e dell'iperglicemia e valutazione del diabete complicazioni.
I pazienti devono essere informati di informare i loro medici se sono in gravidanza o se intendono rimanere incinta.
Ogni dose di Byetta deve essere somministrata come iniezione SC nella coscia, nell'addome o nella parte superiore del braccio in qualsiasi momento 60 minuti prima dei pasti del mattino e della sera (o prima dei due pasti principali della giornata, circa 6 ore o più) a parte). Byetta non deve essere somministrato dopo un pasto. Se si dimentica una dose, il regime di trattamento deve essere ripreso come prescritto con la successiva dose programmata.
Il rischio di ipoglicemia aumenta quando Byetta viene usato in associazione con un agente che induce ipoglicemia, come una sulfonilurea. I sintomi, il trattamento e le condizioni che predispongono allo sviluppo dell'ipoglicemia devono essere spiegati al paziente. Sebbene le normali istruzioni del paziente per la gestione dell'ipoglicemia non debbano essere modificate, queste istruzioni dovrebbero essere rivisto e rafforzato quando si inizia la terapia con Byetta, in particolare se somministrato in concomitanza con una sulfonilurea (vedere PRECAUZIONI, Ipoglicemia).
I pazienti devono essere informati che il trattamento con Byetta può comportare una riduzione dell'appetito, del cibo assunzione e / o peso corporeo e che non è necessario modificare il regime di dosaggio a causa di ciò effetti. Il trattamento con Byetta può anche provocare nausea, in particolare all'inizio della terapia (vedere REAZIONI AVVERSE).
Il paziente deve leggere il foglietto illustrativo "Informazioni per il paziente" e il Manuale per l'utente della penna prima di iniziare la terapia con Byetta e rivederli ogni volta che la prescrizione viene ricaricata. Il paziente deve essere istruito sull'uso e la conservazione corretti della penna, sottolineando come e quando impostare una nuova penna e notare che è necessario solo un passaggio di impostazione al primo utilizzo. Il paziente deve essere avvisato di non condividere la penna e gli aghi.
I pazienti devono essere informati che gli aghi per penna non sono inclusi con la penna e devono essere acquistati separatamente. I pazienti devono essere informati della lunghezza e del calibro dell'ago da utilizzare.
Interazioni farmacologiche
L'effetto di Byetta sul rallentamento dello svuotamento gastrico può ridurre l'entità e la velocità di assorbimento dei farmaci somministrati per via orale. Byetta deve essere usato con cautela nei pazienti che assumono farmaci per via orale che richiedono un rapido assorbimento gastrointestinale. Per i farmaci orali che dipendono dalle concentrazioni di soglia per l'efficacia, come contraccettivi e antibiotici, i pazienti devono essere informati di assumere quei farmaci almeno 1 ora prima Iniezione Byetta. Se tali farmaci devono essere somministrati con il cibo, i pazienti devono essere avvisati di prenderli con un pasto o uno spuntino quando Byetta non viene somministrato. L'effetto di Byetta sull'assorbimento e l'efficacia dei contraccettivi orali non è stato caratterizzato.
warfarin
In uno studio di farmacologia clinica controllata condotto su volontari sani, è stato osservato un ritardo nella tmax di warfarin di circa 2 ore quando warfarin è stato somministrato 30 minuti dopo Byetta. Non sono stati osservati effetti clinicamente rilevanti su Cmax o AUC. Tuttavia, dall'introduzione sul mercato ci sono stati alcuni casi segnalati spontaneamente di aumento dell'INR (Rapporto internazionale normalizzato) con l'uso concomitante di warfarin e Byetta, talvolta associati sanguinamento.
Cancerogenesi, mutagenesi, alterazione della fertilità
Uno studio di carcinogenicità di 104 settimane è stato condotto su ratti maschi e femmine a dosi di 18, 70 o 250 mcg / kg / die somministrati mediante iniezione in bolo SC. Adenomi a cellule C benigni della tiroide sono stati osservati nei ratti femmine a tutte le dosi di exenatide. L'incidenza nei ratti femmine è stata dell'8% e del 5% nei due gruppi di controllo e del 14%, 11% e 23% nei gruppi a bassa, media e alta dose con esposizioni sistemiche di 5, 22 e 130 volte, rispettivamente, l'esposizione umana risultante dalla dose massima raccomandata di 20 mcg / die, in base all'area del plasma sotto la curva (AUC).
In uno studio di carcinogenicità di 104 settimane su topi a dosi di 18, 70 o 250 mcg / kg / die somministrati mediante iniezione in bolo SC, non è stata osservata alcuna evidenza di tumori a dosi fino a 250 mcg / kg / giorno, un'esposizione sistemica fino a 95 volte l'esposizione umana risultante dalla dose massima raccomandata di 20 mcg / giorno, in base a AUC.
Exenatide non si è rivelato mutageno o clastogenico, con o senza attivazione metabolica, nel test di mutagenicità batterica di Ames o nel test di aberrazione cromosomica nelle cellule di ovaia di criceto cinese. Exenatide è risultato negativo nel test del micronucleo di topo in vivo.
Negli studi sulla fertilità nei topi con dosi di SC di 6, 68 o 760 mcg / kg / die, i maschi sono stati trattati per 4 settimane prima durante e durante l'accoppiamento e le femmine sono state trattate 2 settimane prima e durante l'accoppiamento fino al giorno della gestazione 7. Non sono stati osservati effetti avversi sulla fertilità a 760 mcg / kg / giorno, un'esposizione sistemica 390 volte l'esposizione umana risultante dalla dose massima raccomandata di 20 mcg / giorno, sulla base dell'AUC.
Gravidanza
Categoria di gravidanza C
Exenatide ha dimostrato di causare una ridotta crescita fetale e neonatale e effetti scheletrici nei topi a esposizioni sistemiche 3 volte l'esposizione umana risultante dalla dose massima raccomandata di 20 mcg / giorno, basato su AUC. Exenatide ha dimostrato di causare effetti scheletrici nei conigli ad esposizioni sistemiche 12 volte l'esposizione umana risultante dalla dose massima raccomandata di 20 mcg / die, in base all'AUC. Non esistono studi adeguati e ben controllati su donne in gravidanza. Byetta deve essere usato durante la gravidanza solo se il potenziale beneficio giustifica il potenziale rischio per il feto.
Nei topi femmine trattati con dosi di SC di 6, 68 o 760 mcg / kg / die a partire da 2 settimane prima e durante l'accoppiamento fino al giorno della gestazione 7, non vi erano fetali avversi effetti a dosi fino a 760 mcg / kg / giorno, esposizioni sistemiche fino a 390 volte l'esposizione umana risultanti dalla dose massima raccomandata di 20 mcg / giorno, sulla base di AUC.
Nei topi in gravidanza a cui sono state somministrate dosi di SC di 6, 68, 460 o 760 mcg / kg / giorno dal giorno della gestazione dal 6 al 15 (organogenesi), palatoschisi (alcuni con buchi) e scheletro irregolare sono state osservate ossificazione di costole e ossa del cranio a 6 mcg / kg / giorno, un'esposizione sistemica 3 volte l'esposizione umana risultante dalla dose massima raccomandata di 20 mcg / kg / giorno, basato su AUC.
In conigli gravidi trattati con dosi di SC di 0,2, 2, 22, 156 o 260 mcg / kg / giorno dalla gestazione dal 6 ° al 18 ° giorno (organogenesi), scheletro irregolare sono state osservate ossificazioni a 2 mcg / kg / giorno, un'esposizione sistemica 12 volte l'esposizione umana risultante dalla dose massima raccomandata di 20 mcg / giorno, basato su AUC.
Nei topi in gravidanza trattati con dosi di SC di 6, 68 o 760 mcg / kg / giorno dal giorno della gestazione 6 al giorno dell'allattamento 20 (svezzamento), è stato osservato un aumento del numero di decessi neonatali nei giorni postpartum 2-4 in madri somministrate 6 mcg / kg / giorno, un'esposizione sistemica 3 volte l'esposizione umana risultante dalla dose massima raccomandata di 20 mcg / giorno, in base all'AUC.
Madri che allattano
Non è noto se exenatide sia escreto nel latte materno. Molti farmaci vengono escreti nel latte materno e, a causa della possibilità di reazioni avverse clinicamente significative nei neonati in allattamento da exenatide dovrebbe essere fatto se interrompere la produzione di latte per il consumo o interrompere il farmaco, tenendo conto dell'importanza del farmaco per l'allattamento donna. Studi sui topi in allattamento hanno dimostrato che exenatide è presente a basse concentrazioni nel latte (inferiore o uguale al 2,5% della concentrazione nel plasma materno dopo somministrazione sottocutanea). Si deve usare cautela quando Byetta viene somministrato a una donna che allatta.
Uso pediatrico
La sicurezza e l'efficacia di Byetta non sono state stabilite nei pazienti pediatrici.
Uso geriatrico
Byetta è stata studiata in 282 pazienti di età pari o superiore a 65 anni e in 16 pazienti di età pari o superiore a 75 anni. Non sono state osservate differenze in termini di sicurezza o efficacia tra questi pazienti e i pazienti più giovani.
superiore
Reazioni avverse
Utilizzare con metformina e / o una sulfonilurea
Nei tre studi clinici controllati della durata di 30 settimane di Byetta sulla metformina e / o sulfonilurea, eventi avversi con un'incidenza del 5% (esclusa l'ipoglicemia; vedere Tabella 3) che si sono verificati più frequentemente nei pazienti trattati con Byetta rispetto ai pazienti trattati con placebo sono riassunti nella Tabella 4.
Tabella 4: Eventi avversi emergenti con trattamento frequente (â ‰ ¥ 5% di incidenza e maggiore incidenza con il trattamento di Byetta) Esclusa l'ipoglicemia *
| BID Placebo N = 483 % |
Tutte le offerte di Byetta N = 963 % |
|
|---|---|---|
| ||
| Nausea | 18 | 44 |
| vomito | 4 | 13 |
| Diarrea | 6 | 13 |
| Sensazione di nervosismo | 4 | 9 |
| Vertigini | 6 | 9 |
| Mal di testa | 6 | 9 |
| Dispepsia | 3 | 6 |
Gli eventi avversi associati a Byetta sono stati generalmente di intensità da lieve a moderata. L'evento avverso più frequentemente riportato, nausea da lieve a moderata, si è verificato in modo dose-dipendente. Con la terapia continua, la frequenza e la gravità sono diminuite nel tempo nella maggior parte dei pazienti che inizialmente hanno manifestato nausea. Eventi avversi segnalati in â ¥ 1,0 al <5,0% dei pazienti trattati con Byetta e riportati più frequentemente rispetto al placebo incluso astenia (principalmente segnalata come debolezza), diminuzione dell'appetito, malattia da reflusso gastroesofageo e iperidrosi. I pazienti negli studi di estensione a 52 settimane hanno manifestato tipi simili di eventi avversi osservati negli studi controllati di 30 settimane.
L'incidenza di astinenza da eventi avversi è stata del 7% per i pazienti trattati con Byetta e del 3% per i pazienti trattati con placebo. Gli eventi avversi più comuni che hanno portato alla sospensione dei pazienti trattati con Byetta sono stati nausea (3% dei pazienti) e vomito (1%). Per i pazienti trattati con placebo, <1% si è ritirato a causa di nausea e 0% a causa di vomito.
Utilizzare con un tiazolidinedione
Nello studio di 16 settimane controllato con placebo sull'aggiunta di Byetta a un tiazolidinedione, con o senza metformina, l'incidenza e il tipo di altri eventi avversi osservati erano simili a quelli osservati negli studi clinici controllati della durata di 30 settimane con metformina e / o a sulfonilurea. Non sono stati segnalati eventi avversi gravi nel braccio placebo. Nel braccio di Byetta sono stati segnalati due eventi avversi gravi, vale a dire dolore toracico (che porta alla sospensione) e polmonite da ipersensibilità cronica.
L'incidenza di astinenza da eventi avversi è stata del 16% (19/121) per i pazienti trattati con Byetta e del 2% (2/112) per i pazienti trattati con placebo. Gli eventi avversi più comuni che hanno portato alla sospensione dei pazienti trattati con Byetta sono stati nausea (9%) e vomito (5%). Per i pazienti trattati con placebo, <1% si è ritirato a causa della nausea. Brividi (n = 4) e reazioni al sito di iniezione (n = 2) si sono verificati solo in pazienti trattati con Byetta. I due pazienti che hanno riportato una reazione al sito di iniezione avevano titoli elevati di anticorpo anti-exenatide.
Dati spontanei
Dall'introduzione sul mercato di Byetta, sono state riportate le seguenti ulteriori reazioni avverse. Poiché questi eventi sono segnalati volontariamente da una popolazione di dimensioni incerte, non è sempre possibile stimare in modo affidabile la loro frequenza o stabilire una relazione causale con l'esposizione al farmaco.
Generale: reazioni nel sito di iniezione; disgeusia; sonnolenza, INR aumentato con l'uso concomitante di warfarin (alcune segnalazioni associate a sanguinamento).
Allergia / Ipersensibilità: prurito generalizzato e / o orticaria, rash maculare o papulare, angioedema; rare segnalazioni di reazione anafilattica.
Gastrointestinale: nausea, vomito e / o diarrea con conseguente disidratazione; distensione addominale, dolore addominale, eruttazione, costipazione, flatulenza, pancreatite acuta.
Patologie renali e urinarie: alterazione della funzionalità renale, inclusa insufficienza renale acuta, peggioramento dell'insufficienza renale cronica, insufficienza renale, aumento della creatinina sierica (vedere PRECAUZIONI).
immunogenicità
Coerentemente con le proprietà potenzialmente immunogene dei farmaci proteici e peptidici, i pazienti possono sviluppare anticorpi anti-exenatide dopo il trattamento con Byetta. Nella maggior parte dei pazienti che sviluppano anticorpi, i titoli anticorpali diminuiscono nel tempo.
Negli studi controllati della durata di 30 settimane di Byetta sulla metformina e / o sulfonilurea, il 38% dei pazienti presentava anticorpi anti-exenatide a basso titolo a 30 settimane. Per questo gruppo, il livello di controllo glicemico (HbA1c) era generalmente paragonabile a quello osservato in quelli senza titoli anticorpali. Un ulteriore 6% dei pazienti presentava anticorpi con titolo più elevato a 30 settimane. In circa la metà di questo 6% (3% del totale dei pazienti trattati con Byetta negli studi controllati di 30 settimane), la risposta glicemica a Byetta è stata attenuata; il resto ha avuto una risposta glicemica paragonabile a quella dei pazienti senza anticorpi.
Nello studio di 16 settimane del componente aggiuntivo di Byetta ai tiazolidinedioni, con o senza metformina, il 9% dei pazienti aveva anticorpi con titolo più elevato a 16 settimane. Rispetto ai pazienti che non hanno sviluppato anticorpi verso Byetta, è stata attenuata in media la risposta glicemica nei pazienti con anticorpi con titolo più elevato.
La risposta glicemica del paziente a Byetta deve essere monitorata. In caso di peggioramento del controllo glicemico o mancato raggiungimento del controllo glicemico mirato, si deve prendere in considerazione una terapia antidiabetica alternativa.
superiore
sovradosaggio
In uno studio clinico di Byetta, tre pazienti con diabete di tipo 2 hanno sperimentato ciascuno un singolo sovradosaggio di 100 mcg di SC (10 volte la dose massima raccomandata). Gli effetti del sovradosaggio comprendono nausea grave, vomito grave e concentrazioni di glucosio nel sangue in rapido calo. Uno dei tre pazienti ha manifestato grave ipoglicemia che richiede la somministrazione parenterale di glucosio. I tre pazienti si sono ripresi senza complicazioni. In caso di sovradosaggio, deve essere iniziato un adeguato trattamento di supporto in base ai segni e sintomi clinici del paziente.
superiore
Dosaggio e amministrazione
La terapia con Byetta deve essere iniziata a 5 mcg per dose somministrata due volte al giorno in qualsiasi momento entro 60 minuti periodo prima dei pasti del mattino e della sera (o prima dei due pasti principali della giornata, circa 6 ore o più) a parte). Byetta non deve essere somministrato dopo un pasto. Sulla base della risposta clinica, la dose di Byetta può essere aumentata a 10 mcg due volte al giorno dopo 1 mese di terapia. Ogni dose deve essere somministrata come iniezione SC nella coscia, nell'addome o nella parte superiore del braccio.
L'uso di Byetta è raccomandato nei pazienti con diabete mellito di tipo 2 che stanno già assumendo metformina, una sulfonilurea, un tiazolidinedione, una combinazione di metformina e una sulfonilurea, o una combinazione di metformina e un tiazolidinedione, e hanno un valore subottimale controllo glicemico. Quando Byetta viene aggiunto alla terapia con metformina o tiazolidinedione, la dose corrente di metformina o tiazolidinedione può essere continuata poiché è improbabile che la dose di metformina o tiazolidinedione richieda un aggiustamento a causa dell'ipoglicemia quando usata con Byetta. Quando Byetta viene aggiunto alla terapia con sulfonilurea, si può prendere in considerazione una riduzione della dose di sulfonilurea per ridurre il rischio di ipoglicemia (vedere PRECAUZIONI, Ipoglicemia).
Byetta è un liquido limpido e incolore e non deve essere usato se compaiono particelle o se la soluzione è torbida o colorata. Byetta non deve essere utilizzato oltre la data di scadenza. Non sono disponibili dati sulla sicurezza o efficacia dell'iniezione endovenosa o intramuscolare di Byetta.
superiore
Conservazione
Prima del primo utilizzo, Byetta deve essere conservato in frigorifero tra 2 ° C e 8 ° C (36 ° F e 46 ° F). Dopo il primo utilizzo, Byetta può essere mantenuto a una temperatura non superiore a 25 ° C (77 ° F). Non congelare. Non usare Byetta se è stato congelato. Byetta dovrebbe essere protetta dalla luce. La penna deve essere eliminata 30 giorni dopo il primo utilizzo, anche se nella penna rimane del farmaco.
superiore
Come viene fornito
Byetta viene fornito come soluzione sterile per iniezione sottocutanea contenente 250 mcg / mL di exenatide. Sono disponibili i seguenti pacchetti:
5 mcg per dose, 60 dosi, 1,2 mL di penna preriempita NDC 66780-210-07
10 mcg per dose, 60 dosi, 2,4 mL di penna preriempita NDC 66780-210-08
SOLO Rx
Prodotto per Amylin Pharmaceuticals, Inc., San Diego, CA 92121
Commercializzato da Amylin Pharmaceuticals, Inc. e Eli Lilly and Company
1-800-868-1190
http://www.Byetta.com
Byetta è un marchio registrato di Amylin Pharmaceuticals, Inc.
© 2007 Amylin Pharmaceuticals, Inc. Tutti i diritti riservati.
ultimo aggiornamento 09/2007
Byetta (Exenatide) Informazioni paziente (in inglese semplice)
Informazioni dettagliate su segni, sintomi, cause, trattamenti del diabete
Le informazioni contenute in questa monografia non intendono coprire tutti i possibili usi, indicazioni, precauzioni, interazioni farmacologiche o effetti avversi. Questa informazione è generalizzata e non è intesa come consulenza medica specifica. Se ha domande sui medicinali che sta assumendo o desidera maggiori informazioni, consultare il medico, il farmacista o l'infermiere.
torna a: Sfoglia tutti i farmaci per il diabete


